在T℃时,向1 L固定体积的密闭容器M中加入2 mol X和1 mol Y,发生如下反应:2X(g)+Y(g)  aZ(g)+W(g) ΔH=-Q kJ/mol(Q>0);该反应达到平衡后,放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小。
aZ(g)+W(g) ΔH=-Q kJ/mol(Q>0);该反应达到平衡后,放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小。
请回答下列问题:
(1)化学计量数a的值为________。
(2)下列能说明该反应达到了化学平衡状态的是________(填序号)。
a.容器内压强一定
b.容器内气体的密度一定
c.容器内Z的分子数一定
d.容器内气体的质量一定
(3)维持T℃温度不变,若起始时向容器M中加入2 mol X、1 mol Y和1 mol Ar(稀有气体不参与反应),则反应达到平衡后放出的热量是________kJ。
(4)维持T℃温度不变,若在一个和原容器体积相等的恒压容器N中加入2 mol X和1 mol Y,发生题给反应并达到平衡,则________(填“M”或“N”)容器中的反应先达到平衡状态,容器中X的质量分数M________N(填“>”、“<”或“=”)。
(5)已知:该反应的平衡常数随温度的变化情况如表所示:
| 温度/℃ | 200 | 250 | 300 | 350 |
| 平衡常数K | 9.94 | 5.2 | 1 | 0.5 |
若在某温度下,2 mol X和1 mol Y在容器M中反应并达到平衡,X的平衡转化率为50%,则该温度为________℃。
(6)维持T℃温度不变,若起始时向容器M中加入4 mol X和6 mol Y,反应达到平衡时容器内的分子数目减少10%,则反应中放出的热量为________kJ。
(14分)(1)1 (2)ac (3)Q1 (4) N > (5) 350 (6) Q
题目分析:(1)该反应是一个放热反应,升高温度平衡向逆反应方向移动,混合气体的平均相对分子质量减小。由于混合气的平均相对分子质量是混合气的质量和混合气的总的物质的量的比值,气体的质量不变,则气体反应物计量数之和大于气体生成物计量数之和,所以a只能等于1。
(2)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,据此可以判断。a、由于反应前后气体的化学计量数之和不相等,因此在反应过程中压强是变化的,而平衡时压强不再发生变化,所以当压强不再发生变化时,可以说明达到平衡状态,故a正确;b、密度是混合气的质量和容器容积的比值,由于是在固定体积的容器中反应,在反应过程中质量和容积始终是不变的,则无论是否达到平衡状态,密度都不变,故b错误;c、反应达到平衡状态时,物质的浓度、含量、质量等不再发生变化,则平衡时容器内Z分子数一定,故c正确;d、反应物和生成物都是气体,无论是否达到平衡状态,容器内气体的质量都一定,故d错误,答案选ac。
(3)若起始时向容器M中加入2molX、1molY和1molAr(稀有气体不参与反应),X和Y的浓度不变,所以其转化率不变,该反应达到平衡状态时,放出的热量不变为Q1kJ。
(4)由于正方应是体积减小的可逆反应,即在恒温恒容条件下,容器内气体的压强是减小的。所以该条件下,恒压与恒容相比,相当于增大压强,压强越大,反应速率越大,反应到达平衡的时间越短,即N容器首先达到平衡状态。增大压强平衡向正反应方向移动,则X的质量分数减小,即M>N。
(5)2molX和1molY在容器M中反应并达到平衡,x的平衡转化率为50%,则平衡时,c(X)=(1−50%)×2moL÷1L=1mol/L。根据方程式可知平衡时c(Y)=1mol/L-1mol/L×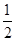 =0.5mol/L。生成Z、W的浓度c(Z)=c(W)=2mol/L×50%×
=0.5mol/L。生成Z、W的浓度c(Z)=c(W)=2mol/L×50%×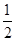 =0.5mol/L。则根据化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值可知,平衡常数K=
=0.5mol/L。则根据化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值可知,平衡常数K=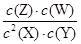 =
=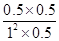 =0.5,所以根据表中数据可知其温度是350℃。
=0.5,所以根据表中数据可知其温度是350℃。
(6)同一容器中,物质的分子数之比等于物质的量之比,当反应达到平衡时容器内的分子数目减少10%时,气体的物质的量减少10%,即气体的物质的量减少(4+6)mol×10%=1mol,根据2X(g)+Y(g)  Z(g)+W(g) ΔH=-Q kJ/mol可知,当气体的物质的量减少1mol时参加反应的X的物质的量是2mol,所以反应中放出的热量为QkJ。
Z(g)+W(g) ΔH=-Q kJ/mol可知,当气体的物质的量减少1mol时参加反应的X的物质的量是2mol,所以反应中放出的热量为QkJ。
