问题
选择题
工业上常用还原沉淀法处理含铬废水(Cr2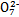 和Cr
和Cr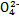 ),其流程为:Cr
),其流程为:Cr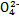
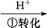 Cr2
Cr2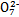
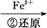 Cr3+
Cr3+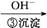 Cr(OH)3↓
Cr(OH)3↓
已知:
(1)步骤①中存在平衡:2Cr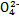 (黄色)+2H+
(黄色)+2H+ Cr2
Cr2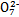 (橙色)+H2O
(橙色)+H2O
(2)步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s) Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)
(3)常温下,Cr(OH)3的溶度积Ksp=10-32;且当溶液中离子浓度小于10-5 mol·L-1时可视作该离子不存在
下列有关说法中正确的是( )
A.步骤①中加酸,将溶液的pH调节至2,溶液显黄色,Cr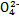 浓度增大
浓度增大
B.步骤①中当2v(Cr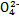 )=v(Cr2
)=v(Cr2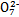 )时,说明反应2Cr
)时,说明反应2Cr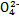 (黄色)+2H+
(黄色)+2H+ Cr2
Cr2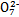 (橙色)+H2O达到平衡状态
(橙色)+H2O达到平衡状态
C.步骤②中,若要还原1 mol Cr2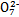 ,需要12 mol (NH4)2Fe(SO4)2·6H2O
,需要12 mol (NH4)2Fe(SO4)2·6H2O
D.步骤③中,当将溶液的pH调节至6时,则可认为废水中的铬已除尽
答案
答案:D
由(1)可知A选项错误;B选项不能判断正、逆反应速率,错误;C选项,1 mol Cr2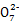 得到6 mol电子,还原1 mol Cr2
得到6 mol电子,还原1 mol Cr2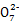 需要6 mol Fe2+,错误;D选项,c(OH-)=10-8 mol·L-1,由Ksp=10-32可得c(Cr3+)=10-8 mol·L-1,正确
需要6 mol Fe2+,错误;D选项,c(OH-)=10-8 mol·L-1,由Ksp=10-32可得c(Cr3+)=10-8 mol·L-1,正确
