某研究小组对一元有机弱酸HA在溶剂苯和水的混合体系中的溶解程度进行研究。在25℃时,弱酸HA在水中部分电离,当HA浓度为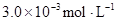 时,其电离度为0.20(电离度=已电离的HA分子数/起始HA的总分子数);在苯中部分发生双聚,生成(HA)2。该平衡体系中,一元有机弱酸HA在溶剂苯(B)和水(W)中的分配系数为K,K=C(HA)B/C(HA)W=1.0,即达到平衡后,以分子形式存在的HA在苯和水两种溶剂中的比例为1:1;其他信息如下:
时,其电离度为0.20(电离度=已电离的HA分子数/起始HA的总分子数);在苯中部分发生双聚,生成(HA)2。该平衡体系中,一元有机弱酸HA在溶剂苯(B)和水(W)中的分配系数为K,K=C(HA)B/C(HA)W=1.0,即达到平衡后,以分子形式存在的HA在苯和水两种溶剂中的比例为1:1;其他信息如下:
| 25℃平衡体系 | 平衡常数 | 焓变 | 起始总浓度 |
在水中,HA 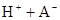 | 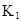 | 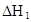 | 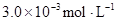 |
在苯中,2HA 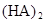 | 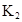 | 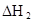 | 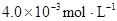 |
回答下列问题:
(1)计算25℃时水溶液中HA的电离平衡常数K1=___________。
(2)25℃,该水溶液的pH为___________,(已知:1g2=0.3,lg3=0.5)在苯体系中HA的转化率为___________。
(3)在苯中,HA发生二聚:2HA (HA)2,反应在较低温度下自发进行,则
(HA)2,反应在较低温度下自发进行,则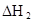 ___________0。
___________0。
(4)25℃混合体系中,HA在苯中发生二聚,若测得某时刻溶液中微粒浓度满足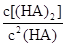 =130,则反应向___________方向进行。
=130,则反应向___________方向进行。
(1)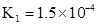 mol/L (2)3.2, 40% (3)< (4)正
mol/L (2)3.2, 40% (3)< (4)正
题目分析:(1)HA在水溶液中电离:HA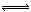 H++A-,根据电离度为0.20,c(H+)=3.0×10-3mol/L×0.20=6.0×10-4mol•L‾1,则K=6.0×10-4mol•L‾1×6.0×10-4mol•L‾1÷(3.0×10-3mol•L‾1—6.0×10-4mol•L‾1)=1.5×10-4mol•L‾1。(2)pH=-lg(H+)=-lg(6.0×10-4)=3.2;达到平衡后,以分子形式存在的HA在苯和水两种溶剂中的比例为1:1,c(HA)=3.0×10-3mol•L‾1—6.0×10-4mol•L‾1=2.4×10-3mol•L‾1,转化的HA为4.0×10-3mol•L‾1—2.4×10-3mol•L‾1=1.6×10-3mol•L‾1,所以在苯体系中HA的转化率为,1.6×10-3mol•L‾÷4.0×10-3mol•L‾1×100% ="40%" 。(3)该反应在较低温度下自发进行,T较小时,∆H-T∆S<0,因为反应物质的量减小,即∆S<0,所以∆H<0。(4)由(2)中数据可算出2HA
H++A-,根据电离度为0.20,c(H+)=3.0×10-3mol/L×0.20=6.0×10-4mol•L‾1,则K=6.0×10-4mol•L‾1×6.0×10-4mol•L‾1÷(3.0×10-3mol•L‾1—6.0×10-4mol•L‾1)=1.5×10-4mol•L‾1。(2)pH=-lg(H+)=-lg(6.0×10-4)=3.2;达到平衡后,以分子形式存在的HA在苯和水两种溶剂中的比例为1:1,c(HA)=3.0×10-3mol•L‾1—6.0×10-4mol•L‾1=2.4×10-3mol•L‾1,转化的HA为4.0×10-3mol•L‾1—2.4×10-3mol•L‾1=1.6×10-3mol•L‾1,所以在苯体系中HA的转化率为,1.6×10-3mol•L‾÷4.0×10-3mol•L‾1×100% ="40%" 。(3)该反应在较低温度下自发进行,T较小时,∆H-T∆S<0,因为反应物质的量减小,即∆S<0,所以∆H<0。(4)由(2)中数据可算出2HA (HA)2的平衡常数K=8.0×10-4mol•L‾1÷(2.4×10-3mol•L‾1)2=146,
(HA)2的平衡常数K=8.0×10-4mol•L‾1÷(2.4×10-3mol•L‾1)2=146,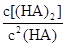 =130<K,所以反应向正反应方向进行。
=130<K,所以反应向正反应方向进行。
