氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟制备氨基甲酸铵,并探究其分解反应平衡常数。反应的化学方程式: 2NH3(g)+CO2(g)  NH2COONH4(s)。请按要求回答下列问题:
NH2COONH4(s)。请按要求回答下列问题:
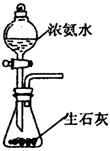
(1)请在下图1方框内画出用浓氨水与生石灰制取氨气的装置简图。
(2)制备氨基甲酸铵的装置如下图2所示。生成的氨基甲酸铵小晶体悬浮在四氯化碳中。
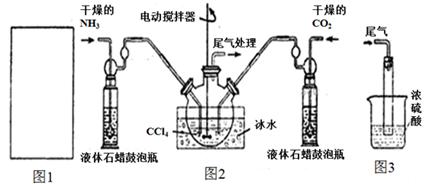
①从反应后的混合物中分离出产品的实验方法是_____________(填操作名称)。
②上图3中浓硫酸的作用是_______________________________________。
(3)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡。实验测得不同温度下的平衡数据列于下表:
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
①下列选项可以判断该分解反应达到平衡的是________。
A.
B.密闭容器内物质总质量不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
②该分解反应的焓变ΔH______0(填 “>”、“=”或“<”),25.0℃时分解平衡常数的值=__________。
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量将_________(填“增加”,“减少”或“不变”)。
(1)
(2)①过滤 ②吸收未反应的氨气,防止空气中的水蒸气进入反应器使氨基甲酸铵水解
(3)①AC ②> ; 1.6×10-8(或1.6384×10-8); 增加
题目分析:题目分析:(1)浓氨水与生石灰制取氨气,反应不需要加热,所以正确的装置图可以是 。
。
(2)①由于生成的氨基甲酸铵小晶体悬浮在四氯化碳中,所以从反应后的混合物中分离出产品的实验方法是过滤。
②反应中氨气过滤,所以浓硫酸的作用是吸收未反应的氨气。另外氨基甲酸铵易水解,所以浓硫酸还起到防止空气中的水蒸气进入反应器使氨基甲酸铵水解的作用。
(3)①在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。A、反应速率的方向相反,且满足反应速率之比是相应的化学计量数之比,可以说明反应达到平衡状态,A正确;B、根据质量守恒定律可知,密闭容器内物质总质量始终不变,B不能说明反应达到平衡状态;C、密度是混合气的质量和容器容积的比值,在反应过程中容积始终是不变的,但气体的质量是变化的,所以当密度不再发生变化时可以说明达到平衡状态,C正确; D、混合气中氨气和CO2的体积之比始终是2:1的,即氨气体积分数始终不变,因此不能说明反应达到平衡状态,故D错误,答案选AC。
②根据表中数据可知,随着温度的升高,气体的压强增大,这说明升高温度平衡向生成氨气和CO2的方向进行,即分解反应是吸热反应,因此该分解反应的焓变ΔH>0;根据反应NH2COONH4(s) 2NH3(g)+CO2(g)可知,n(NH3)=2n(CO2),则根据表中数据可知,c(NH3)=2c(CO2)=4.8×10-3mol/L×
2NH3(g)+CO2(g)可知,n(NH3)=2n(CO2),则根据表中数据可知,c(NH3)=2c(CO2)=4.8×10-3mol/L×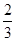 =3.2×10-3mol/L,所以依据平衡常数的表达式,25.0℃时氨基甲酸铵的分解平衡常数为K=c2(NH3)×c(CO2)=(3.2×10-3mol/L)2×1.6×10-3mol/L=1.6×10-8(mol/L)3。
=3.2×10-3mol/L,所以依据平衡常数的表达式,25.0℃时氨基甲酸铵的分解平衡常数为K=c2(NH3)×c(CO2)=(3.2×10-3mol/L)2×1.6×10-3mol/L=1.6×10-8(mol/L)3。
③压缩容器体积,增大了压强,平衡向逆反应方向移动,氨基甲酸铵固体的质量增加。