问题
选择题
反应:NH4HS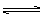 NH3(气)+H2S(气),在某一温度下达到平衡,下列各种情况中,不能使平衡发生移动的是
NH3(气)+H2S(气),在某一温度下达到平衡,下列各种情况中,不能使平衡发生移动的是
A.其他条件不变,通入SO2气体
B.移去一部分NH4HS固体,其他条件不变
C.温度和体积不变,通入氮气
D.温度和压强不变,通入氮气
答案
B、C
A.SO2与H2S的反应生成S,使[H2S]减小,平衡向右移动。B.NH4HS是固体,其浓度是常量,与其多少无关,所以减少或增加NH4HS平衡不移动。C、D.N2本身与平衡体系中各物质不反应,所以若容器体积不变,则NH3,H2S的浓度不变,平衡不移动;若容器体积增大(压强不变即体积增大),由H2S,NH3的浓度减小,平衡向右移动。故答案为B、C。
