问题
选择题
相同温度下,体积均为0.5 L的两个恒容密闭容器中发生可逆反应:
2XY2(g)+Y2(g)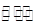 2XY3(g),
2XY3(g), 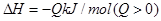
实验测得反应在起始、达到平衡时的有关数据如下表所示:
| 容器 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| 编号 | XY2 | Y2 | XY3 | |
| ① | 2 | 1 | 0 | 放热0.25QkJ |
| ② | 1.2 | 0.6 | 0.8 | |
A.达到平衡时,①和②两容器中气体的平均相对分子质量相同
B.容器②中反应达到平衡时放出的热量为0.15 Q kJ
C.达到平衡时,两个容器中Y2的物质的量浓度均为1.5 mol·L-1
D.若容器①的其他条件不变,只增加1mol稀有气体,则达到平衡时放出的热量等于0.25 Q kJ
答案
答案:B
由容器①放热量可知,平衡时各物质消耗量(生成量)为:XY2:0.5mol, Y:0.25mol, XY3:0.5mol,剩余量为:XY2:1.5mol, Y:0.75mol, XY3:0.5mol,则平衡时浓度为:XY2:3mol/L, Y:1.5mol/L, XY3:1mol/L,K值为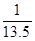 。C描述正确,不选。
。C描述正确,不选。
从起始时各物质物质的量可知,两容器达到平衡时是等效平衡,平衡时各物质浓度相同,所以A描述正确,不选。
又由两容器为等效平衡,容器②若要达到平衡,则需要生成0.3molXY2和0.15molY,平衡前反应逆向进行程度更大,达到平衡需吸收热量,B错误。
若容器①其他条件不变,充入稀有气体,虽然会增大压强,但是此压强变化不会影响各反应物浓度,对反应平衡没有任何影响,D描述正确,不选。
