问题
填空题
T℃时,A气体与B气体反应生成C气体,反应过程中A、 B、C浓度变化如图(I)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(II)所示。
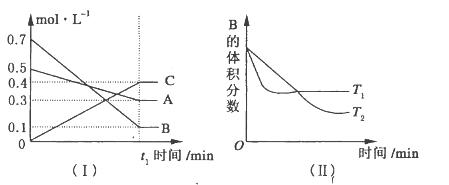
根据以上条件,回答下列问题:
(1)A与B反应生成C的化学方程式为_________________________________________,
正反应为_________________________(填“放热”或“吸热”)反应。
(2)t1min后,改变下列某—条件,能使平衡向逆反应方向移动的有___________(填字母编号)。
A.保持其他条件不变,增大压强
B.保持容器总体积不变,通入少量稀有气体
C.保持其他条件不变,升高温度
答案
(共6分)(1)A(g)+3B(g) 2C(g) (2分) 放热 (2分)
2C(g) (2分) 放热 (2分)
(2)C (2分)
题目分析:(1)由图(Ⅰ)知在一定时间内,A、B、C浓度的变化量之比等于1:3:2,所以A与B反应生成C的化学方程式为A(g)+3B(g) 2C(g),由图(Ⅱ)结合“先拐先平”的规律知T1>T2,说明温度升高,B的体积分数增大,平衡逆向移动,正向为放热反应;
2C(g),由图(Ⅱ)结合“先拐先平”的规律知T1>T2,说明温度升高,B的体积分数增大,平衡逆向移动,正向为放热反应;
(2)A、增大压强平衡正向移动,错误;B、容器总体积不变,通入少量稀有气体,各物质的浓度不变,平衡不移动,错误;C、升温,平衡逆向移动,正确,答案选C。
