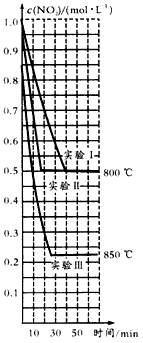
在2L密闭容器内,反应2NO2(g)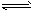 NO(g)+O2(g)在三种不同的条件下进行实验,其中实验I、Ⅱ都是在800℃,实验Ⅲ是在850℃;NO、O2的起始浓度都为0,NO2的起始浓度都为1.0 mol/L,NO2的浓度随时间的变化关系如下图所示。请回答下列问题:
NO(g)+O2(g)在三种不同的条件下进行实验,其中实验I、Ⅱ都是在800℃,实验Ⅲ是在850℃;NO、O2的起始浓度都为0,NO2的起始浓度都为1.0 mol/L,NO2的浓度随时间的变化关系如下图所示。请回答下列问题:
(1)①该反应的平衡常数表达式为:K=______________________。 ②下列叙述不能说明该反应已达到平衡状态的是______________。
a.v正(NO2)=2v逆(O2)
b.c(NO2) =c(NO)
c.气体的平均摩尔质量不变
d.NO的体积分数保持不变
(2)①对比实验I、Ⅱ和Ⅲ,得出的下列结论正确的是________。
a.实验Ⅱ和I相比,可能隐含的条件是:反应容器的体积缩小了
b.实验Ⅱ和I相比,可能隐含的条件是:使用了效率更高的催化剂
c.实验I的平衡常数大于实验Ⅲ的平衡常数
d.对比实验I和Ⅲ可知,该可逆反应的正反应是放热反应
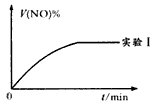
②下图是实验I中NO体积分数V%随时间t的变化曲线,请在图中补画实验Ⅲ中NO体积分数V%随时间t的变化曲线。
(3)实验I,从反应开始到平衡时,v(O2)=_________ mol/(L·min)。若实验I中将NO2的起始浓度改为1.2 mol/L,其他条件不变,NO2的转化率将______________(填“增大”“减少”或“不变”)。
(4)若实验I平衡后,再向该2L密闭容器中通入1molNO2与l mol NO、0.5molO2组成的混合气体,则平衡将________移动(填“向右”“向左”“不”或“无法确定”)。 再次达到平衡后,__________ mol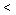 n(NO)
n(NO)  _________mol。
_________mol。
(1)① ②b
②b
(2)①b②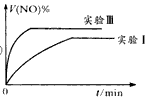
(3)6.25×10-3 mol/(L·min);减少
(4)向左;1;2
