(6分)如图所示,当关闭阀门K时,向甲中充入1.5 mol A、3.5 mol B,向乙中充入 3 mol A、7 mol B,起始时,甲、乙体积均为V L。在相同温度和有催化剂存在的条件下,两容器中各自发生下列反应:3A(g)+2B(g)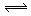 C(g)
C(g) +2D(g);ΔH<0
+2D(g);ΔH<0
达到平衡(Ⅰ)时,V(乙)=0.86V L。
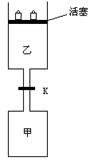
请回答:
(1)乙中B的转化率为 ;
(2)甲中D和乙中C的物质的量比较: (填“相等”、“前者大”、“后者大”);
(3)打开K,过一段时间重新达平衡(Ⅱ)时,乙的体积为 (用含V的代数式表示,连通管中气体体积忽略不计。)
(1)20% (2)后者大 (3)0.72V
(1) 3A(g)+2B(g) C(g)
C(g) +2D(g)
+2D(g)
起始量(mol) 3 7 0 0
转化量(mol) 3x 2x x 2x
平衡量(mol) 3-3x 7-2x x 2x
则
解得2x=1.4
所以B转化率是1.4÷7×100%=20%
(2)甲是保持等温等容的,而乙是保持等温等压的。又因为反应是体积减小的可逆反应,所以乙中反应物的转化率高于甲中反应物的转化率,因此乙中C的物质的量多。
(3)打开K,则相当于是等温等压下的可逆反应,因此和原来乙中平衡是等效的。此时消耗B是10.5mol×0.2=2.1mol,则消耗A是2.1mol÷2×3=3.15mol,生成C和D分别是1.05mol和2.1mol,如果设平衡时容器的总体积是X,则有

解得X=1.72VL
所以乙的体积为1.72VL-VL=0.72V。
