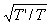问题
选择题
在密闭容器中,将1.0 mol CO与1.0 mol H2O混合加热到800 ℃,发生下列反应:
CO(g)+H2O(g)  CO2(g)+H2(g)。一段时间后该反应达到平衡,测得CO的物质的量为0.5 mol。则下列说法正确的是( )
CO2(g)+H2(g)。一段时间后该反应达到平衡,测得CO的物质的量为0.5 mol。则下列说法正确的是( )
A.800 ℃下,该反应的化学平衡常数为0.25
B.427 ℃时该反应的平衡常数为9.4,则该反应的ΔH>0
C.800 ℃下,若继续向该平衡体系中通入1.0 mol的CO(g),则平衡时CO物质的量分数为33.3%
D.800 ℃下,若继续向该平衡体系中通入1.0 mol的H2O(g) ,则平衡时CO转化率为66.7%
答案
答案:D
CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)
起始(mol) 1.0 1.0 0 0
平衡(mol) 1.0-x 1.0-x x x
则1.0-x=0.5 x=0.5 mol
A项:K=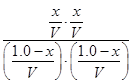 =1,错误;B项,温度降低,K增大,平衡右移,正反应为放热反应,错误;C项,
=1,错误;B项,温度降低,K增大,平衡右移,正反应为放热反应,错误;C项,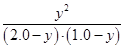 =1,y=
=1,y= mol,CO的质量分数:
mol,CO的质量分数: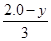 ×100%≈44.4%,错误;D项,根据C项分析,D项正确。
×100%≈44.4%,错误;D项,根据C项分析,D项正确。