用氮化硅(Si3N4)陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:
3SiCl4(g)+2N2(g)+6H2(g)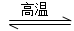 Si3N4(s)+12HCl(g) ΔH<0
Si3N4(s)+12HCl(g) ΔH<0
完成下列填空:
(1)在一定温度下进行上述反应,若反应容器的容积为2 L,3 min后达到平衡,测得固体的质量增加了2.80 g,则H2的平均反应速率为________mol/(L·min);该反应的平衡常数表达式K=________。
(2)上述反应达到平衡后,下列说法正确的是________。
a.其他条件不变,压强增大,平衡常数K减小
b.其他条件不变,温度升高,平衡常数K减小
c.其他条件不变,增大Si3N4物质的量平衡向左移动
d.其他条件不变,增大HCl物质的量平衡向左移动
(3)一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是________。
a.3v逆(N2)=v正(H2)
b.v正(HCl)=4v正(SiCl4)
c.混合气体密度保持不变
d.c(N2):c(H2):c(HCl)=1:3:6
(4)若平衡时H2和HCl的物质的量之比为m/n,保持其他条件不变,降低温度后达到新的平衡时,H2和HCl的物质的量之比________m/n(填“>”、“=”或“<”)。
(1)0.02 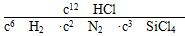
(2)bd (2)ac (4)<
(1)反应达到平衡后,Δn(Si3N4)=2.80/140=0.02 mol ,故
v(H2)=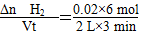 =0.02 mol/(L·min)。
=0.02 mol/(L·min)。
(2)平衡常数是温度的函数,与压强无关,故a错误;温度升高,平衡逆向移动,K减小,故b正确;增大固体物质的物质的量,平衡不移动,故c错误;增大n(HCl),平衡逆向移动K减小,故d正确。
(3)a项,表示v正=v逆,故正确;b项,均为v正,故错误;c项,由于容器密闭恒容,且该反应前后气体的物质的量发生改变,当混合气体的密度不变时,则各气体的物质的量不再变化,说明反应已经达到平衡状态,故正确;d项,当各物质的浓度比等于化学计量数之比时,不能表示反应已达到平衡状态,故错误。
(4)温度降低,平衡正向移动,n(H2)减小,n(HCl)增大,故达到新平衡时 。
。
