300°C时,将2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g) 2C(g)+2D(g) ΔH=Q,2 min末达到平衡,生成0.8 mol D。
2C(g)+2D(g) ΔH=Q,2 min末达到平衡,生成0.8 mol D。
(1)300°C时,该反应的平衡常数表达式为K=________。已知K300°C<K350°C,则ΔH________0(填“>”或“<”)。
(2)在2 min末时,B的平衡浓度为_______,D的平均反应速率为_______。
(3)若温度不变,缩小容器容积,则A的转化率________(填“增大”“减小”或“不变”),原因是__________________________________________。
(4)如果在相同的条件下,上述反应从逆反应方向进行,开始时若加入C、D各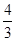 mol。若使平衡时各物质的物质的量浓度与原平衡相同,则还应该加入B________mol。
mol。若使平衡时各物质的物质的量浓度与原平衡相同,则还应该加入B________mol。
(1)  >
>
(2)0.8 mol·L-1 0.2 mol·L-1·min-1
(3)不变 反应前后气体的总物质的量不变,压强对平衡无影响
(4)4/3
(1)若温度越高,K越大,则说明升温,平衡正向移动,即正反应为吸热反应,ΔH>0。(2)生成0.8 mol D,则反应掉0.4 mol B,剩余1.6 mol B,c(B)=1.6 mol÷2 L=0.8 mol·L-1。v(B)=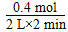 =0.1 mol·L-1·min-1,由化学计量数知,D的反应速率应为B的2倍,故v(D)=2v(B)=2×0.1 mol·L-1·min-1=0.2 mol·L-1·min-1。(3)该反应为反应前后气体的总物质的量不变的反应,加压平衡不移动,故A的转化率不变。(4)将C、D折算成A、B,则相当于加入2 mol A和2/3 mol B,容器体积固定,若浓度相同,则说明起始时物质的量相等,故B还应加入2 mol-
=0.1 mol·L-1·min-1,由化学计量数知,D的反应速率应为B的2倍,故v(D)=2v(B)=2×0.1 mol·L-1·min-1=0.2 mol·L-1·min-1。(3)该反应为反应前后气体的总物质的量不变的反应,加压平衡不移动,故A的转化率不变。(4)将C、D折算成A、B,则相当于加入2 mol A和2/3 mol B,容器体积固定,若浓度相同,则说明起始时物质的量相等,故B还应加入2 mol-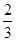 mol=
mol=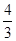 mol。
mol。
