一定温度下某容积固定的密闭容器中加入2 mol A和1 mol B,发生如下反应:2A(g)+B(g)  3C(g)+D(s) ΔH=-Q kJ·mol-1(Q>0),当反应达到平衡后,反应放出的热量为Q1 kJ,物质A的转化率为α。请回答下列问题:
3C(g)+D(s) ΔH=-Q kJ·mol-1(Q>0),当反应达到平衡后,反应放出的热量为Q1 kJ,物质A的转化率为α。请回答下列问题:
(1)Q1________Q(填“<”、“>”或“=”),理由是__________________________。
(2)A的转化率α=________(用含Q、Q1的代数式表示);平衡后,若加入少量物质D,A的转化率会________(填“增大”、“减小”或“不变”)。
(3)反应达到平衡后,若升高温度,K________(填“增大”、“减小”或“不变”),混合气体的平均相对分子质量________(填“增大”、“减小”或“不变”)。
(4)维持温度不变,若起始时向容器中加入的物质如下列四个选项,则反应达到平衡后放出的热量仍为Q1 kJ的是(稀有气体不参与反应)________(填字母)。
A.2 mol A、1 mol B、1 mol Ar
B.3 mol C、1 mol D
C.1 mol A、0.5 mol B、1.5 mol C、0.5 mol D
D.2 mol A、1 mol B、1 mol D
(1)< 该反应是可逆反应,2 mol A和1 mol B不可能完全反应
(2)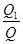 ×100% 不变
×100% 不变
(3)减小 增大
(4)AD
本题综合考查了反应热、转化率、化学平衡移动等之间的关系,虽然综合性强,但每一问难度并不是很大,运用解化学平衡类试题的基本技巧即可顺利求解。因是可逆反应,2 mol A和1 mol B不可能完全反应,故Q1<Q,此时A的转化率α=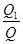 ×100%;平衡后,若加入少量物质D,由于D是固体,浓度不变,故A的转化率不变。因为是放热反应,升高温度,平衡逆向移动,K减小;升高温度时气体质量增大,气体物质的量不变,故混合气体的平均相对分子质量增大;选项A、B、C、D所达平衡状态与原平衡均等效,但只有A、D选项达平衡时放出的热量与原平衡相等。
×100%;平衡后,若加入少量物质D,由于D是固体,浓度不变,故A的转化率不变。因为是放热反应,升高温度,平衡逆向移动,K减小;升高温度时气体质量增大,气体物质的量不变,故混合气体的平均相对分子质量增大;选项A、B、C、D所达平衡状态与原平衡均等效,但只有A、D选项达平衡时放出的热量与原平衡相等。
