问题
选择题
一定条件下的密闭容器中:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH=-905.9 kJ/mol,下列叙述正确的是( )
4NO(g)+6H2O(g) ΔH=-905.9 kJ/mol,下列叙述正确的是( )
A.4 mol NH3和5 mol O2反应,达到平衡时放出的热量为905.9 kJ
B.平衡时v正(O2)=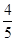 v逆(NO)
v逆(NO)
C.平衡后降低压强,混合气体平均摩尔质量增大
D.平衡后升高温度,混合气体中NO含量降低
答案
答案:D
由于该反应为可逆反应,故反应达平衡时反应物不能全部转化为生成物,放出的热量小于905.9 kJ,A错误;根据速率之比等于化学计量数之比可知反应达平衡时,v正(O2)= v逆(NO),B错误;降低压强,平衡右移,气体的物质的量增大,但气体的质量不变,故混合气体的摩尔质量减小,C错误;升高温度,平衡左移,NO的含量降低,D正确。
v逆(NO),B错误;降低压强,平衡右移,气体的物质的量增大,但气体的质量不变,故混合气体的摩尔质量减小,C错误;升高温度,平衡左移,NO的含量降低,D正确。
