I.800℃时,向容积为2L的恒容密闭容器中充入一定量的CO和H2O维持恒温,发生反应CO(g)+H2O(g) H2(g)+CO2(g),反应过���中测定的部分数据见下表:
H2(g)+CO2(g),反应过���中测定的部分数据见下表:
| 反应时间/min | 0 | 2 | 4 | 6 |
| n(CO)/mol | 1.20 | 0.90 | 0.80 | |
| n(H2O)/ mol | 0.60 | 0.20 |
②800℃时,化学平衡常数K的值为______________;
③保持其他条件不变,向平衡体系中再通入0.20 mol H2O,与原平衡相比,达到新平衡时CO转化率______(填“增大”或“减小”或“不变”)。
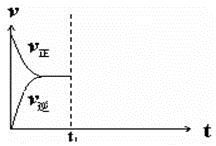
④在恒温恒压密闭容器中通入CO和H2O各1 mol发生该反应,当反应达到平衡后,维持温度与压强不变,t1时再通入各1 mol的CO和H2O的混合气体,请在下图中画出正(v正)、逆(v逆)反应速率在t1后随时间t变化的曲线图。
II.实验室中利用复分解反应制取Mg(OH)2。实验数据和现象如下表所示(溶液体积均取用1mL):

①现象III是 ;
②如果向0.028 mol/L的MgCl2溶液中加入等体积的NaOH溶液,请计算NaOH溶液的浓度至少达到 mol/L时,溶液中开始出现白色沉淀(Ksp(Mg(OH)2)= 5.6×10-12)。
③MgCl2溶液和氨水混合后存在下列化学平衡:
Mg2+(aq) + 2NH3·H2O(aq) 2NH4+(aq) + Mg(OH)2(s)该反应化学平衡常数的表达式为K= ,列出该反应平衡常数K与Kb(NH3·H2O)、Ksp(Mg(OH)2)的关系式 。
2NH4+(aq) + Mg(OH)2(s)该反应化学平衡常数的表达式为K= ,列出该反应平衡常数K与Kb(NH3·H2O)、Ksp(Mg(OH)2)的关系式 。
Ⅰ①0.075 mol·L-1·min-1 ②1 ③增大
④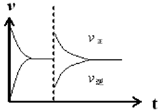
Ⅱ①生成白色沉淀 ②4×10-5 mol·L-1③K=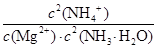 ;K=
;K=
Ⅰ.①根据表中数据可知,反应在2 min时CO的物质的量减少了1.20mol-0.90mol=0.30mol。根据方程式可知,水蒸气的物质的量也减少0.30mol,其浓度是0.30mol÷2L=0.15mol/L,所以2min内的平均速率为v(H2O)=0.15mol/2min=0.075 mol·L-1·min-1。
②2min时水蒸气的物质的量是0.30mol,3min时是0.20mol,减少0.10mol,则3min时CO的物质的量是0.80mol。由于4min时CO的物质的量也是0.8mol,这说明反应在3min时达到平衡状态,则
CO(g)+H2O(g)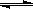 H2(g) + CO2(g)
H2(g) + CO2(g)
起始物质的浓度(mol/L) 0.60 0.30 0 0
变化物质的量浓度(mol/L) 0.20 0.20 0.20 0.20
平衡物质的量浓度(mol/L) 0.40 0.10 0.20 0.20
所以平衡常数K=0.20×0.20/0.40×0.10=1.0
③保持其他条件不变,向平衡体系中再通入0.20 mol H2O,增大水蒸气的浓度,平衡向正反应方向进行,因此CO的转化率增大。
④维持温度与压强不变,t1时再通入各1 mol的CO和H2O的混合气体,则容器的容积必然增大。由于反应前后体积不变,所以平衡是等效的。但正反应速率增大,逆反应速率减小,而平衡状态不变,因此正确的图像是
 。
。
Ⅱ①根据表中数据可知,实验Ⅲ和Ⅳ相比,氨水的浓度相同,实验Ⅲ中氯化镁的浓度高于实验Ⅳ中氯化镁的浓度。由于实验Ⅳ中有白色沉淀氢氧化镁生成,所以所以Ⅲ中一定生成白色沉淀氢氧化镁。
②设NaOH溶液的浓度至少达到x,则混合物后溶液中是OH-浓度0.5x。由于混合后溶液中镁离子浓度是0.014mol/L,所以要生成氢氧化镁沉淀,则(0.5x)2·0.014≥5.6×10-12,解得x≥4×10-5mol/L。
③化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以根据方程式可知,该可逆反应的平衡常数K=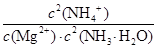 。K=
。K=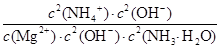 =
=