一定温度下,在4个容积均为1 L的恒容容器中分别进行反应(各容器中A都足量)A(s)+B(g) C(g)+D(g) ΔH ="+100" kJ·mol-1,某时刻测得部分数据如下表:
C(g)+D(g) ΔH ="+100" kJ·mol-1,某时刻测得部分数据如下表:
| 容器编号 | n(B)/mol | n(C)/mol | n(D)/mol | 反应时间/min | 反应速率 |
| Ⅰ | 0.06 | 0.60 | 0.10 | t1 | v(正)=v(逆) |
| Ⅱ | 0.12 | 1.20 | 0.20 | t2 | |
| Ⅲ | 0.32 | 1.0 | 0 | 0 | |
| Ⅳ | 0.12 | 0.30 | v(正)=v(逆) |
下列说法正确的是
A.容器Ⅰ中平均反应速率v(B)=0.04/t1 mol·L-1·min-1
B.t2时容器Ⅱ中v(正)>v(逆)
C.容器Ⅲ中反应至平衡时吸热20 kJ
D.容器Ⅳ中c(D)= 0.4 mol·L-1
答案:D
题目分析:A.化学反应速率的在单位时间内物质浓度的改变值。只知道某时刻该物质是物质的量,而不知道其物质的量的改变数值,所以无法计算其反应速率。错误。B.t2时容器Ⅱ中由于不清楚反应进行的方向,所以无法确定v(正)与v(逆)的相对大小。错误。C.容器Ⅲ中反应从什么方向开始不清楚,所以无法确定达到平衡时吸热的多少。错误。D.由于容器Ⅰ与容器Ⅳ中都是同一温度下的平衡状态。所以K相等。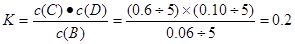 。所以
。所以 解得x="c(D)=" 0.4 mol·L-1。正确。
解得x="c(D)=" 0.4 mol·L-1。正确。