环境中常见的重金属污染物有:汞、铅、锰、铬、镉。处理工业废水中含有的Cr2O72-和CrO42-,常用的方法为还原沉淀法,该法的工艺流程为CrO42-H+①转化Cr2O72-Fe2+②还原Cr3+OH-③沉淀Cr(OH)3↓。
其中第①步存在平衡2CrO42- (黄色)+2H+ Cr2O72- (橙色)+H2O。
Cr2O72- (橙色)+H2O。
(1)写出第①步反应的平衡常数表达式 。
(2)关于第①步反应,下列说法正确的是 。
A.通过测定溶液的pH可以判断反应是否已达到平衡状态
B.该反应为氧化还原反应
C.强酸性环境,溶液的颜色为橙色
(3)第②步中,还原0.1 mol Cr2O72-,需要 mol的FeSO4·7H2O。
(4)第③步除生成Cr(OH)3外,还可能生成的沉淀为 。
(5)在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)  Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,当c(Cr3+)降至10-5 mol/L,认为c(Cr3+)已经完全沉淀,现将第③步溶液的pH调至4,请通过计算说明Cr3+是否沉淀完全(请写出计算过程): 。
Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,当c(Cr3+)降至10-5 mol/L,认为c(Cr3+)已经完全沉淀,现将第③步溶液的pH调至4,请通过计算说明Cr3+是否沉淀完全(请写出计算过程): 。
(1)K=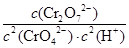
(2)AC
(3)0.6
(4)Fe(OH)3
(5)当pH调至4时,c(OH-)=10-10 mol/L,c(Cr3+)=10-32/c3(OH-) =10-2 mol/L>10-5 mol/L,因此Cr3+没有沉淀完全
(1)因H2O是纯液态物质,其浓度视为常数,故第①步反应的平衡常数表达式为K=c(Cr2O72-)/[c2(CrO42-)·c2(H+)]。
(2)利用反应①可知,反应正向进行时,溶液pH增大,故pH不变时说明反应达到平衡,A项正确;CrO42-和Cr2O72-中Cr均为+6价,该反应不是氧化还原反应,B项错误;在酸性环境中,溶液中c(Cr2O72-)较大,溶液呈橙色,C项正确。
(3)在第②步反应中Cr2O72-被还原为Cr3+,0.1 mol Cr2O72-被还原时转移电子的物质的量为0.1 mol×2×(6-3)=0.6 mol,而还原剂Fe2+被氧化为Fe3+,故需要消耗0.6 mol FeSO4·7H2O。
(4)在第②步反应中Fe2+被氧化为Fe3+,故第③步还有Fe(OH)3生成。
