问题
填空题
在一个2 L的密闭容器中,加入3 mol A和1 mol B,发生下述反应:
3A(g)+B(g)2C(g)+3D(s),5 min达到平衡时,C的浓度为0.6 mol/L。
(1)达到平衡时,A的转化率为 ,此温度下的平衡常数K= 。
(2)维持容器的温度不变,若缩小容器的体积,则平衡将向 (填“正反应方向移动”“逆反应方向移动”或“不移动”)。
(3)维持容器的体积和温度不变,向密闭容器中加入氦气,达到新平衡时,B、C的浓度之比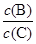 将 (填“增大”、“减小”或“不变”)。
将 (填“增大”、“减小”或“不变”)。
(4)当增加A的浓度,B的转化率 ;若将C分离出来,化学平衡常数 。(填“增大”、“减小”或“不变”)
答案
(1)60% 8.33 (2)正反应方向移动 (3)不变 (4)增大 不变
(1)根据各物质的速率之比等于化学计量数之比,也等于各物质的物质的量及浓度变化之比的原则进行“三段法”计算。
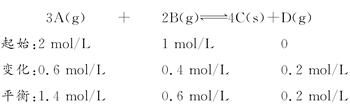
(2)温度不变而缩小容器体积,相当于加压,由于D为固体,正反应方向是气体体积减少的方向,所以平衡右移。
(3)由于维持体系的温度、容积不变,充入氦气不改变平衡中各物质的浓度,平衡不移动。
(4)若增加A的浓度,平衡右移,B的转化率增大;对于一个平衡来讲,平衡常数仅与温度有关,与浓度无关。
