温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g) PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据如图:
PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据如图:
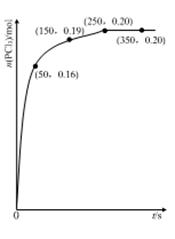
下列说法正确的是
A.反应在前50 s 的平均速率v(PCl3)=0.0032 mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol·L-1,则反应的△H<0
C.相同温度下,起始时向容器中充入2.0 mol PCl3和2.0mol Cl2,达到平衡时,PCl3的转化率小于80%
D.相同温度下,起始时向容器中充入1.0 mol PCl5、0.20mol PCl3和0.20 mol Cl2,反应达到平衡前v(正)>v(逆)
答案:D
题目分析:A、反应在前50 s 的平均速率v(PCl3)=0.16÷2÷50="0.0016" mol·L-1·s-1,错误;B、平衡时c(PCl3)=0.20÷2=0.10mol·L-1,升高温度其浓度增大,平衡正向移动,反应吸热,错误;C、相同温度下,起始时向容器中充入1.0 mol PCl3和1.0 mol Cl2时与元平衡为等效平衡, PCl3的转化率小于80% ,充入2.0 mol PCl3和2.0 mol Cl2,压强增大平衡向生成PCl5方向移动,PCl3的转化率增大,错误;
PCl5(g) PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)
始量 1 0 0
转化量 0.2 0.2 0.2
平衡量 0.8 0.2 0.2
k=(0.2/2×0.2/2)÷0.8/2=0.025
此时浓度熵Q=(0.2/2×0.2/2)÷1.0/2=0.02<0.025,平衡正向移动,v(正)>v(逆),正确。
