甲醇燃料分为甲醇汽油和甲醇柴油。工业上合成甲醇的方法很多。
(1)一定条件下发生反应:
①CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H1
②2CO(g)+O2(g) =2CO2(g) △H2
③2H2(g)+O2(g)=2H2O(g) △H3
则CO(g) + 2H2(g)  CH3OH(g) △H= 。
CH3OH(g) △H= 。
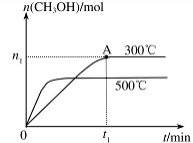
(2)在容积为2L的密闭容器中进行反应: CO(g)+2H2(g) CH3OH(g) ,其他条件不变,在300℃和500℃时,物质的量n(CH3OH)与反应时间t的变化曲线如图所示。该反应的△H 0(填>、<或=)。
CH3OH(g) ,其他条件不变,在300℃和500℃时,物质的量n(CH3OH)与反应时间t的变化曲线如图所示。该反应的△H 0(填>、<或=)。
(3)若要提高甲醇的产率,可采取的措施有____________(填字母)。
A.缩小容器体积
B.降低温度
C.升高温度
D.使用合适的催化剂E.将甲醇从混合体系中分离出来
(4)CH4和H2O在催化剂表面发生反应CH4+H2O CO+3H2,T℃时,向1 L密闭容器中投入1 mol CH4和1 mol H2O(g),5小时后测得反应体系达到平衡状态,此时CH4的转化率为50% ,计算该温度下的平衡常数 (结果保留小数点后两位数字)。
CO+3H2,T℃时,向1 L密闭容器中投入1 mol CH4和1 mol H2O(g),5小时后测得反应体系达到平衡状态,此时CH4的转化率为50% ,计算该温度下的平衡常数 (结果保留小数点后两位数字)。
(5)以甲醇为燃料的新型电池,其成本大大低于以氢为燃料的传统燃料电池,目前得到广泛的研究,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:
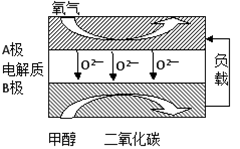
①B极的电极反应式为 。
②若用该燃料电池做电源,用石墨做电极电解硫酸铜溶液,当电路中转移1mole-时,实际上消耗的甲醇的质量比理论上大,可能原因是 。
(6)25℃时,草酸钙的Ksp=4.0×10-8,碳酸钙的Ksp=2.5×10-9。向20ml碳酸钙的饱和溶液中逐滴加入8.0×10-4 mol·L-1的草酸钾溶液20ml,能否产生沉淀 (填“能”或“否”)。
(1)△H1+1/2△H2-1/2△H3
(2 <
(3)ABE
(4)6.75
(5)① CH3OH+3O2-6e-= CO2+ 2H2O;
②甲醇不完全被氧化,生成C或CO 或电池能量转化率达不到100%
(6)否
(1)①+1/2②—1/2③。整理可得:CO(g)+ 2H2(g) CH3OH(g)△H=△H1+1/2△H2-1/2△H3。
CH3OH(g)△H=△H1+1/2△H2-1/2△H3。
(2)由图像可以看出:升高温度,平衡时CH3OH的含量降低,说明升高温度,化学平衡向逆反应方向移动,根据平衡移动原理,升高温度化学平衡向吸热反应方向移动,逆反应方向为吸热反应,所以正反应为放热反应。因此△H<0。
(3)若要提高甲醇的产率,应该使平衡正向移动。由于该反应的正反应为气体体积缩小的放热反应,根据平衡移动原理,降低温度、增大压强(即缩小容器体积)增大反应物的浓度或把甲醇从反应体系中分离出来。因此选项为A、B、E。
(4)根据反应方程式CH4+H2O CO+3H2中各种物质的相互关系及甲烷的转化率可知:当反应达到平衡时,c(CH4)=0.5mol/L;c(H2O)=0.5mol/L;c(CO)=0.5mol/L;c(H2)=1.5mol/L.化学平衡状态是可逆反应达到平衡状态时,各种生成物浓度幂指数的乘积一各种反应物浓度幂指数乘积的比,所以
CO+3H2中各种物质的相互关系及甲烷的转化率可知:当反应达到平衡时,c(CH4)=0.5mol/L;c(H2O)=0.5mol/L;c(CO)=0.5mol/L;c(H2)=1.5mol/L.化学平衡状态是可逆反应达到平衡状态时,各种生成物浓度幂指数的乘积一各种反应物浓度幂指数乘积的比,所以
 。
。
(5)①通入甲醇的电极B为原电池的负极, B极的电极反应式为CH3OH + 3O2-6e-= CO2+ 2H2O; 通入氧气的电极为正极,正极发生反应:O2+ 4e-= 2O2-。
②当电路中转移1mole-时,实际上消耗的甲醇的质量比理论上大,可能原因是甲醇不完全被氧化,生成C或CO或电池能量转化率达不到100%等。
(6)碳酸钙的Ksp=2.5×10-9,则c(Ca2+)·c(CO32-)=Ksp, c(Ca2+)=Ksp1/2=(2.5×10-9)1/2=5×10-5,当向20ml碳酸钙的饱和溶液中逐滴加入8.0×10-4 mol·L-1的草酸钾溶液20ml 时,c(Ca2+)·c(C2O42-)=(1/2×5×10-5) ×(1/2×8.0×10-4)=10-8,小于草酸钙的Ksp=4.0×10-8,所以不能产生草酸钙沉淀。