问题
选择题
下列说法不正确的是
A.在固定体积的密闭容器中发生可逆反应A(s)+B(g) C(g)+D(g),当混合气体的密度不再改变时,说明已达到化学平衡状态
C(g)+D(g),当混合气体的密度不再改变时,说明已达到化学平衡状态
B.对于反应C(s)+CO2(g) 2CO(g)△H>0,改变某一条件,若化学平衡常数增大,则反应速率也一定增大
2CO(g)△H>0,改变某一条件,若化学平衡常数增大,则反应速率也一定增大
C.向0.1mol·L-1的NH3·H2O中加入氯化铵固体,则溶液中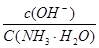 增大
增大
D.常温下向Mg(OH)2悬浊液中加入MgCl2浓溶液后,溶液中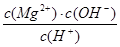 不变
不变
答案
答案:C
在反应A(s)+B(g) C(g)+D(g)中, A是固体,反应容器体积固定,故达到平衡前气体的密度随气体质量变化而变化,当气体密度不再改变时,说明已达到化学平衡状态,A正确;△H>0,说明反应C(s)+CO2(g)
C(g)+D(g)中, A是固体,反应容器体积固定,故达到平衡前气体的密度随气体质量变化而变化,当气体密度不再改变时,说明已达到化学平衡状态,A正确;△H>0,说明反应C(s)+CO2(g)  2CO(g)是吸热反应,化学平衡常数增大,说明反应温度升高,因而反应速率也一定增大,B正确;氨水中存在电离平衡:NH3·H2O
2CO(g)是吸热反应,化学平衡常数增大,说明反应温度升高,因而反应速率也一定增大,B正确;氨水中存在电离平衡:NH3·H2O NH4++OH-,加入氯化铵固体后增大了c(NH4+),平衡向左移动,c(OH-)减小而c(NH3·H2O)增大,故
NH4++OH-,加入氯化铵固体后增大了c(NH4+),平衡向左移动,c(OH-)减小而c(NH3·H2O)增大,故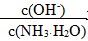
减小,C错误;Mg(OH)2悬浊液中存在着溶解平衡
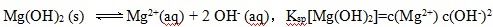
故
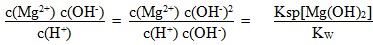 ,
,
而Ksp[Mg(OH)2]与KW均是温度的函数,不随浓度变化而改变,D正确。
