氢能被视为未来的理想清洁能源,科学家预测“氢能”将是21世纪最理想的新能源。目前分解水制氢气的工业制法之一是“硫—碘循环”,主要涉及下列反应:
Ⅰ SO2+2H2O+I2= H2SO4+2HI Ⅱ 2HI H2+I2
H2+I2
Ⅲ 2H2SO4= 2SO2↑+O2↑+2H2O
(1)分析上述反应,下列判断正确的是 。
a.反应Ⅲ易在常温下进行 b.反应I中SO2还原性比HI强
c.循环过程中需补充H2O d.循环过程中产生1molO2的同时产生1molH2
(2)一定温度下,向2L密闭容器中加入1mol HI(g),发生反应Ⅱ,H2物质的量随时间的变化如图所示。0—2min内的平均反应速率v(HI)= 。该温度下,反应2HI(g) H2(g)+I2(g)的平衡常数K= 。相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则 是原来的2倍。
H2(g)+I2(g)的平衡常数K= 。相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则 是原来的2倍。

a.平衡常数 b.HI的平衡浓度
c.达到平衡的时间 d.平衡时H2的体积分数
(3)SO2在一定条件下可被氧化生成SO3,其反应为:2SO2 (g) + O2(g)  2SO3(g) △H<0。某科研单位利用原电池原理,用SO2和O2来制备硫酸,装置如图,电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触。
2SO3(g) △H<0。某科研单位利用原电池原理,用SO2和O2来制备硫酸,装置如图,电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触。
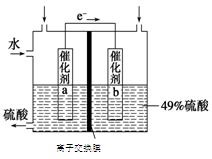
①a电极的电极反应式为 ;
②若得到的硫酸浓度仍为49%,则理论上参加反应的SO2与加入的H2O的质量比为 。
(4)实际生产还可以用氨水吸收SO2生成亚硫酸的铵盐。现取a克该铵盐,若将其中的SO2全部反应出来,应加入10 mol/L的硫酸溶液的体积范围为 。
(1)bc(2分)
(2)0.05mol·L-1·min-1(2分);1.56×10-2或1/64(2分);b (2分)
(3)①SO2 +2H2O-2e-=SO42-+ 4H+(2分) ②8∶15(2分)
(4) (a/1160)L~(a/1980)L (3分)
题目分析:(1)反应Ⅲ,2H2SO4==2SO2↑+O2↑+2H2O,硫酸是高沸点,在常温下不易分解,a不正确;反应I,SO2+2H2O+I2= H2SO4+2HI中,反应物SO2还原性比产物HI强,b正确;循环过程中H2O被分解为H2和O2,故需补充H2O不正确;由H2O被分解可知产生1molO2的同时产生2molH2,D不正确。
(2)v(HI)= 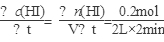 =0.05mol·L-1·min-1。该温度下,反应2HI(g)
=0.05mol·L-1·min-1。该温度下,反应2HI(g) H2(g)+I2(g)到达平衡时,c(H2)=c(I2)= 0.1mol·L-1,c(HI)= 0.8mol·L-1的平衡常数K=
H2(g)+I2(g)到达平衡时,c(H2)=c(I2)= 0.1mol·L-1,c(HI)= 0.8mol·L-1的平衡常数K=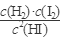 =1.56×10-2。相同温度下,若开始加入HI(g)的物质的量是原来的2倍,温度不变平衡常数不变;加压平衡不移动,故HI的平衡浓度是原来的2倍;浓度最大,速率加快,达到平衡的时间少于原来的2倍;平衡时H2的体积分数不变。
=1.56×10-2。相同温度下,若开始加入HI(g)的物质的量是原来的2倍,温度不变平衡常数不变;加压平衡不移动,故HI的平衡浓度是原来的2倍;浓度最大,速率加快,达到平衡的时间少于原来的2倍;平衡时H2的体积分数不变。
(3)①a电极得到电子,物质被氧化,故是SO2通入的电极,反应式为SO2 +2H2O-2e-=SO42-+ 4H+;
②理论上2SO2+2H2O+O2==2H2SO4,硫酸浓度仍为49%假设49g即0.5mol H2SO4,需要SO2是0.5mol、H2O是0.5mol,硫酸溶液中还有水51g,理论上参加反应的SO2与加入的H2O的质量比为0.5mol×32g·mol-1:(0.5mol×18g·mol-1+51g)=8:15。
(4)实际生产还可以用氨水吸收SO2生成亚硫酸的铵盐。即(NH4)2SO3或NH4HSO3现取a克该铵盐,让它们分别于硫酸溶液反应,可计算出体积范围为(a/1160)L~(a/1980)L。
