(16分)碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是理想,更是一种值得期待的新的生活方式,请运用化学反应原理的相关知识研究碳及其化合物的性质。
(1)近年来,我国储氢纳米碳管研究取得重大进展,用电弧法合成的碳纳米管中常伴有大量碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法提纯,其反应化学方程式为:
____C+____K2Cr2O7 + ====___CO2↑+ ____K2SO4 + ____Cr2(SO4)3+ ____H2O
请完成并配平上述化学方程式。
其中氧化剂是________________,氧化产物是_________________
(2)甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产。工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
CO(g)+ 2H2(g) CH3OH(g)△H1=-116 kJ·mol-1
CH3OH(g)△H1=-116 kJ·mol-1
①已知: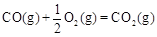 △H2=-283 kJ·mol-1
△H2=-283 kJ·mol-1
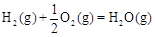 △H3=-242 kJ·mol-1
△H3=-242 kJ·mol-1
则表示1mol气态甲醇完全燃烧生成CO 2和水蒸气时的热化学方程为 ;
②在容积为1L的恒容容器中,分别研究在230℃、250℃、270℃三种温度下合成甲醇的规律。下图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。请回答:
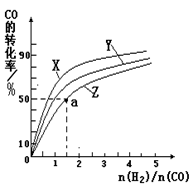
ⅰ)在上述三种温度中,曲线Z对应的温度是
ⅱ)利用图中a点对应的数据,计算出曲线Z在对应温度下CO(g)+ 2H2(g) CH3OH(g)的平衡常数K= 。
CH3OH(g)的平衡常数K= 。
③在某温度下,将一定量的CO和H2投入10L的密闭容器中,5min时达到平衡,各物质的物质的浓度(mol•L-1)变化如下表所示:
| 0min | 5min | 10min | |
| CO | 0.1 | 0.05 | |
| H2 | 0.2 | 0.2 | |
| CH3OH | 0 | 0.04 | 0.05 |
(1)3 2 8 H2SO4 3 2 2 8 (3分,填上H2SO41分,配平2分)
K2Cr2O7(1分),CO2(1分)
(2)①CH3OH(g)+3/2O2(g)= CO2(g)+ 2H2O(g) △H=-651kJ·mol-1(3分)
②ⅰ)270℃(2分) ⅱ) 4 L2 /mol2(2分,没单位不扣分)
③增大H2的浓度(2分);增大了0.1 mol•L-1(2分)
题目分析:
(1)从____C+____K2Cr2O7 + ==___CO2↑+ ____K2SO4 + ____Cr2(SO4)3+ ____H2O式用原子守恒法分析,所缺的物质当属H2SO4,先标出变价元素的化合价,利用电子得失相等进行配平,最后利用原子守恒将其它物质配平即可;在有元素化合价下降的反应物都为氧化剂,含有化合价升高的元素的生成物都是氧化产物,从化合价角度判断。
(2)①先写出甲醇燃烧的方程式,标明各物质的状态,利用盖斯定律求得焓变。
ⅰ)根据甲醇的合成方程式,其为放热反应,所以温度高不利于一氧化碳的转化,转化率低的温度较高,所以Z线为270℃
ⅱ) 由坐标中读出CO的转化率为50%,n(H2)/n(CO)=1.5,可设n(CO)=amol,则n(H2)=1.5amol
依题意得,体积为1L CO(g) + 2H2(g)  CH3OH(g)
CH3OH(g)
起始: a mol/L 1.5a mol/L 0
变化: 0.5 mol/L a mol/L 0.5 mol/L
平衡: 0.5 mol/L 0.5 mol/L 0.5 mol/L
K= c(CH3OH)/c(CO)·c2(H2)=" 0.5" mol/L÷0.5 mol/L÷(0.5mol/L)2=4L2/mol2
③由题意中提示“只改变了一个条件”,结合起始量和10min时达到平衡的各物质的量,可知,H2的物质的量还是0.2mol ,可知改变的量当为增加了H2的物质的量,而增加了多少则要从10min时的恢复至起始状态
依题意得 CO(g) + 2H2(g)  CH3OH(g)
CH3OH(g)
起始: 0.1 mol/L 0.3 mol/L 0
变化:
平衡: 0.05 mol/L 0.2mol/L 0.05 mol/L
则起始的氢气浓度当为 0.3 mol/L,对比之前的浓度,所以增加的氢气的量为0.1 mol•L-1