问题
选择题
下列实验过程中曲线变化不正确的是
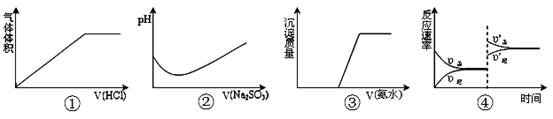
A.①表示Na2CO3溶液中滴入稀盐酸
B.②表示溴水中滴入Na2SO3溶液
C.③表示HCl和MgCl2溶液中滴入氨水
D.④表示一定条件下反应:2SO2+O2 2SO3 ΔH< 0 ,达平衡后,增大压强
2SO3 ΔH< 0 ,达平衡后,增大压强
答案
答案:A
题目分析:A.反应CO32-+H+=HCO3- HCO3-+H+=CO2↑+H2O,开始时没有气体产生,错误;B.Br2+SO32-+H2O=2Br-+SO42-+2H+,前一段时间有溴存在的时候,由方程式可知PH会下降,但当溴反应完后,由于亚硫酸钠是强碱弱酸盐显碱性,继续加入则PH上升,正确;C.氨水先和HCl反应,再和MgCl2溶液反应,所以在有盐酸存在时,没有沉淀产生,正确;D.增大压强,同时增大正逆反应速率,同时平衡向着体积减小的方向移动,即向正反应方向移动,所以正反应速率大于逆反应速率,正确。
