问题
填空题
已知工业制氢气的反应为:CO(g)+H2O(g) CO2(g)+H2(g)反应过程中能量变化如图所示。在500℃时的平衡常数K=9。若在2L的密闭容器中CO和水蒸气的起始浓度都是0.1 mol/L,10 min时达到平衡状态。
CO2(g)+H2(g)反应过程中能量变化如图所示。在500℃时的平衡常数K=9。若在2L的密闭容器中CO和水蒸气的起始浓度都是0.1 mol/L,10 min时达到平衡状态。

(1)增加H2O(g)的浓度,CO的转化率将_____(填“增大”“减小”或“不变”)。
(2)平衡常数的表达式K=_________。400℃时的平衡常数K________9 (填“>”“<”或“=”)。
(3)500℃时,10 min内v(H2O)=____,在此过程中体系的能量_____(填“增加”或“减少”)______kJ。
(4)已知2H2(g)+O2(g)=2H2O(g) △H= -484 kJ/mol 结合上图写出CO完全燃烧生成CO2的热化学方程式:
__________________。
答案
(1)增大;
(2)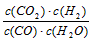 ;>
;>
(3)0.0075 mol/(L·min);减少;6.15
(4)CO(g)+ O2(g)=CO2(g) △H=-283kJ/mol
