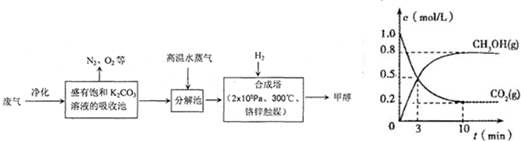
为解决大气中CO2的含量增大的问题,某科学家提出“绿色自由”构想:把工厂排出的富含CO2的废气经净化吹入碳酸钾溶液吸收,然后再把CO2从溶液中提取出来,经化学反应使废气中的CO2转变为燃料甲醇.“绿色自由”构想的部分技术流程如下:
(1)合成塔中反应的化学方程式为______;△H<0.从平衡移动原理分析,低温有利于提高原料气的平衡转化率.而实际生产中采用300℃的温度,除考虑温度对反应速率的影响外,还主要考虑了______.
(2)从合成塔分离出甲醇的原理与下列______操作的原理比较相符(填字母).
A.过滤 B.分液 C.蒸馏 D.结晶
(3)工业流程中一定包括“循环利用”,“循环利用”是提高效益、节能环保的重要措施.“绿色自由”构想技术流程中能够“循环利用”的,除K2CO3溶液和CO2、H2外,还包括______.
(4)在体积为2L的合成塔中,充入2mol CO2和6mol H2,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.从反应开始到平衡,v(H2)=______;能使平衡体系中n(CH3OH)/n(CO2)增大的措施有______.
(5)如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4.巳知CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H1=-890.3kJ/mol,H2 (g)+
O2(g)=H2O(l)△H2=-285.8kJ/mol写出CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式______.1 2
(1)合成塔中的反应是二氧化碳和氢气在一定条件下可生成甲醇和水,其方程式为:CO2+3H2
CH3OH+H2O;一定条件
温度影响催化剂的活性,除考虑温度对反应速率的影响外,还主要考虑了催化剂的催化活性,
故答案为:CO2+3H2
CH3OH+H2O;催化剂的催化活性;一定条件
(2)分离沸点相差比较大,互溶的液体,可以用蒸馏的方法进行分离,故选:C;
(3)由工艺流程可知,可重复利用的物质有K2CO3溶液和CO2、H2、高温水蒸气,故答案为:高温水蒸气;
(4)由图可知,10min达平衡,平衡时甲醇的浓度为0.8mol/L,
所以v(CH3OH)=
=0.08mol/(L•min),反应速率之比等于化学计量数之比,所以v(H2)=3v(CH3OH)=3×0.08mol/(L•min)=0.24mol/(L•min).0.8mol/L 10min
增大H2的用量、减少生成H2O 的量等,平衡右移,可以增大n(CH3OH)/n(CO2)的值,
故答案为:0.24mol/(L•min);增大H2的用量等;
(5)巳知:①CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H1=-890.3kJ/mol,
②H2 (g)+
O2(g)=H2O(l)△H2=-285.8kJ/mol,1 2
则CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式可
根据盖斯定律②×4-①得CO2(g)+4H2 (g)=CH4(g)+2H2O(l)△H=-252.9kJ/mol,
故答案为:CO2(g)+4H2 (g)=CH4(g)+2H2O(l)△H=-252.9kJ/mol.
