问题
选择题
已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g),△H=+49.0kJ•mol-1
②CH3OH(g)+
O2(g)=CO2(g)+2H2(g),△H=-192.9kJ•mol-11 2
下列说法正确的是( )
A.CH3OH转变成H2的过程一定要吸收能量
B.①反应中,反应物的总能量高于生成物总能量
C.根据②推知反应:CH3OH(l)+
O2(g)=CO2(g)+2H2(g)的△H>-192.9kJ•mol-11 2
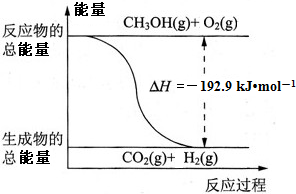
D.反应②中的能量变化如图所示
答案
A、反应①是吸热反应,反应②是放热反应,CH3OH转变成H2的过程不一定要吸收能量,故A错误;
B、①CH3OH(g)+H2O(g)=CO2(g)+3H2(g),△H=+49.0kJ•mol-1,反应是吸热反应,生成物能量高于反应物,故B错误;
C、CH3OH(l)变化为CH3OH(g)需要吸热,CH3OH(l)+
O2(g)=CO2(g)+2H2(g)的△H>-192.9 kJ•mol-1 ,故C正确;1 2
D、物质的量不同焓变不同,图象不能反映反应过程,故D错误;
故选C.
