问题
选择题
氢气在氧气中燃烧产生蓝色火焰。已知破坏1molH-H键消耗的能量为Q1kJ,破坏1molO = O键消耗的能量为Q2kJ,形成1molH-O键释放的能量为Q3kJ。则下列关系式中正确的是
A.2Q1+ Q2 > 4Q3
B.2Q1+Q2<4Q3
C.Q1 +Q2 <Q3
D.Q1+Q2=Q3
答案
答案:B
氢气在氧气中燃烧属于放热反应,其反应方程式为: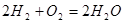 ,即可得2Q1+Q2<4Q3
,即可得2Q1+Q2<4Q3
氢气在氧气中燃烧产生蓝色火焰。已知破坏1molH-H键消耗的能量为Q1kJ,破坏1molO = O键消耗的能量为Q2kJ,形成1molH-O键释放的能量为Q3kJ。则下列关系式中正确的是
A.2Q1+ Q2 > 4Q3
B.2Q1+Q2<4Q3
C.Q1 +Q2 <Q3
D.Q1+Q2=Q3
答案:B
氢气在氧气中燃烧属于放热反应,其反应方程式为: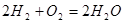 ,即可得2Q1+Q2<4Q3
,即可得2Q1+Q2<4Q3