问题
计算题
已知2H2(g)+O2(g)→2H2O(g) ΔH= -484KJ/mol;2H2(g)+O2(g)→2H2O(l) ΔH= -572KJ/mol
若在标准状况下,将H2和O2组成的混合气体点燃爆炸后,再恢复到标准状况下,气体总体积减少33.6升,计算反应过程中放出的热量是多少?(要求简要解析)
答案
286KJ
根据方程式可知2H2(g)+O2(g)=2H2O(l),每生成2mol水,气体体积就减少3mol。实际减少的是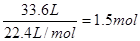 ,所以应该生成水的物质的量是1mol。所以放出的热量是
,所以应该生成水的物质的量是1mol。所以放出的热量是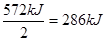 。
。
