问题
选择题
已知16g硫变成硫蒸汽需要吸收akJ的热量,而2mol硫蒸汽完全燃烧会放出bkJ的热量,则下列热化学方程式正确的是
A.S(s) + O2(g) =SO2(g);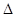 H=-
H=-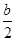 kJ/mol
kJ/mol
B.S(g) + O2(g) =SO2(g);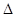 H=-
H=-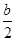 kJ/mol
kJ/mol
C.S(s) + O2(g) =SO2(g);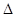 H=-(2a-
H=-(2a-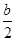 )kJ/mol
)kJ/mol
D.S(s) + O2(g) =SO2(g);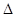 H=-(b-a)kJ/mol
H=-(b-a)kJ/mol
答案
答案:B
2mol硫蒸汽完全燃烧会放出bkJ的热量,所以选项B正确,A不正确。16g硫变成硫蒸汽需要吸收akJ的热量,所以固态硫燃烧的热化学方程式为S(s) + O2(g) =SO2(g); 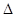 H=-(
H=-(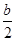 -2a)kJ/mol,因此CD都是错误的。答案选B。
-2a)kJ/mol,因此CD都是错误的。答案选B。
