问题
选择题
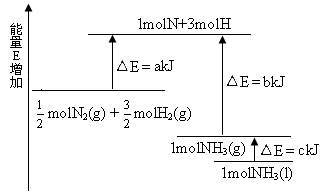
化学反应N2+3H2=2NH3的能量变化如下图所示,该反应的热化学方程式是( )
A.N2(g)+3H2(g) ="==" 2NH3(1)△H=2(a-b-c)kJ·mol-1
B.N2(g)+3H2(g) ="==" 2NH3(g)△H=2(b-a)kJ·mol-1
C.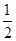 N2(g)+
N2(g)+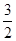 H2(g) ===NH3(1)△H=(b+c-a)kJ·mol-1
H2(g) ===NH3(1)△H=(b+c-a)kJ·mol-1
D.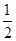 N2(g)+
N2(g)+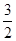 H2(g) ===NH3(g)△H=(a+b)kJ·mol-1
H2(g) ===NH3(g)△H=(a+b)kJ·mol-1
答案
答案:A
根据图像可知,反应物的总能量高于生成物的总能量,因此是放热反应。每生成1mol氨气放出的热量是(b+c-a)kJ。所以正确的答案是A。
