问题
选择题
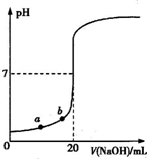
用0.1000mol•L-1 NaOH溶液滴定20.00mL未知浓度的盐酸(酚酞作指示剂)的滴定曲线如图所示.下列说法正确的是( )
A.水电离出的氢离子浓度:a>b
B.盐酸的物质的量浓度为0.0100mol•L-1
C.指示剂变色时,说明盐酸与NaOH恰好完全反应
D.当滴加NaOH溶液10.00 mL(忽略反应前后体积变化),该混合液的pH=1+lg3
答案
A.a点时加入NaOH较少,溶液中c(H+)较大,c(H+)越大,水的电离程度越小,则有水电离出的氢离子浓度:a<b,故A错误;
B.加入NaOH溶液20.00mL时,酸碱恰好中和,由c(酸)×V(酸)=c(碱)×V(碱)可知,盐酸的物质的量浓度为0.100 mol•L-1,故B错误;
C.指示剂为酚酞,溶液变色范围为8.2~10,溶液呈碱性,NaOH过量,并不是恰好完全反应,故C错误;
D.当滴加NaOH溶液10.00 mL时,酸过量,c(H+)=
=0.02L×0.1mol/L-0.01L×0.1mol/L 0.03L
×10-1mol/L,则pH=1+lg3,故D正确.1 3
故选D.
