(8分)已知1mol CO气体完全燃烧生成CO2气体,放出283KJ热量,1mol氢气完全燃烧生成液态水放出286KJ热量,1mol CH4气体完全燃烧生成CO2气体和液态水放出890KJ热
(1)写出H2燃烧热的热化学方程式 。
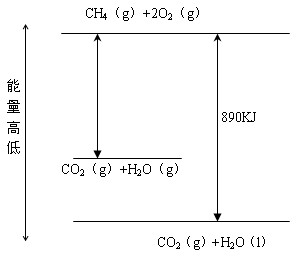
(2)若1mol CH4气体完全燃烧生成CO2气体和水蒸汽,放出热量 890KJ(填“=”、“>”“<”)
(3)若将a mol CH4,CO,H2混合气体完全燃烧,生成CO2气体和液态水,则放出热量(Q)的取值范围是 。
(4)若将a mol CH4,CO,H2混合气体完全燃烧,生成CO2气体和液态水,且CO2和H2O物质的量相等,则放出热量(Q)的取值范围是 。
⑴ H2(g) +1/2O2(g) =H2O(l);△H=-286kJ·mol-1
⑵ < ⑶ 283a kJ < Q <890a kJ ⑷ 284.5a kJ < Q < 586.5a kJ
(1)燃烧热是在一定条件下1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量
(2)参照下图:
(3)由题给数据,三气体各为1 mol完全燃烧放出的热量最大为890kJ,最少为283kJ。
(4)生成的CO2和液态H2O的物质的量相等,可用极值假设分析,有以下几种可能
①若无CO,生成的CO2和液态H2O的物质的量不可能相等,故不合题意
②若无H2, CO和CH4各为a/2摩尔符合题意,放出的热量(Q)=a/2(283+890)=586.5aKJ
③若无CH4,可能CO和H2各为a/2摩尔符合题意,放出的热量(Q)=a/2(283+286)="284.5akJ" ,
若只有一种气体均不可能;
综合信息可知:放出的热量(Q)的取值范围为:284.5aKJ<Q<586.5aKJ
