问题
选择题
已知热化学方程式:
① C2H2(g) +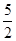 O2(g) == 2CO2(g)+H2O(l) ΔH1=-1301.0 kJ•mol-1
O2(g) == 2CO2(g)+H2O(l) ΔH1=-1301.0 kJ•mol-1
② C(s)+ O2(g) == CO2(g) △H2=-393.5 kJ•mol-1
③ H2(g)+  O2(g) == H2O(1) △H3 =" -285.8" kJ·mol-1
O2(g) == H2O(1) △H3 =" -285.8" kJ·mol-1
则反应④ 2C(s)+ H2(g) == C2H2(g)的△H为( )
A.+228.2 kJ·mol-1
B.-228.2 kJ·mol-1
C.+1301.0 kJ·mol-1
D.+621.7 kJ·mol-1
答案
答案:A
题目分析:根据盖斯定律可知,②×2+③-①即得到反应④ 2C(s)+ H2(g) == C2H2(g),所以该反应的△H=-393.5 kJ•mol-1×2-285.8 kJ·mol-1+1301.0 kJ•mol-1=+228.2 kJ·mol-1,答案选A。
点评:根据热化学方程式计算反应热时,一般依据盖斯定律进行。
