问题
填空题
(4分)已知25℃、101kpa时,CH3OH(l)的燃烧热为726.5 KJ/mol。
⑴写出该条件下CH3OH(l)完全燃烧的热化学方程式: 。
⑵已知有关反应的能量变化如下图,则反应CH4+H2O(g) CO+3H2的焓变△H=_______。
CO+3H2的焓变△H=_______。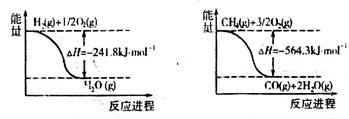
答案
(1)CH3OH(l) + 3/2O2(g) = CO2(g) + 2H2O(l);△H=" -726.5KJ/mol" (2分)
(2) 161.1 KJ·mol-1(2分)
题目分析:(1)热化学方程,要注意指明反应时的温度和压强,其次,方程中所有的反应物和产物都用括号注明它们在反应时的状态。燃烧,属于放热反应,故△H<0,此热化学方程式为
CH3OH(l) + 3/2O2(g) = CO2(g) + 2H2O(l);△H= -726.5KJ/mol。
(2)盖斯定律:化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关。
由图可知H2+(1/2)O2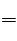 H2O △H="-24.18KJ/mol" ① CH4+(3/2)O2
H2O △H="-24.18KJ/mol" ① CH4+(3/2)O2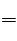 CO+2H2O △H=-564.3KJ/mol②
CO+2H2O △H=-564.3KJ/mol②
既有H2O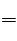 H2+(1/2)O2 △H="24.18KJ/mol" ③
H2+(1/2)O2 △H="24.18KJ/mol" ③
③×3+②
得CH4+H2O(g) CO+3H2 △H=" 161.1" KJ·mol-1
CO+3H2 △H=" 161.1" KJ·mol-1
点评:此题考核了热力学方程和盖斯定律,要求学生在书写的时候,要注意热力学方程的书写格式。
