问题
填空题
(8分)(1)已知断开1 mol H2中的化学键需吸收436 kJ热量,断开1 mol Cl2中的化学键需要吸收243 kJ能量,而形成1 molHCl分子中的化学键要释放431 kJ能量,试求1 mol H2与1 mol Cl2反应的能量变化。△H= 。
(2)已知常温时,0.1mol/L某一元酸HA在水中有0.1%发生电离,则该溶液的PH=___①___,此酸的电离平衡常数K=___②___,由HA电离出来的H+的浓度约为水电离出来的H+的浓度的__③__倍。
答案
(1) -183 KJ.mol-1 (2) 4, 1×10-7 ,106
题目分析:(1)反应热等于反应物的键能之和与产物的键能之和,则△H=436 kJ.mol-1+243 kJ.mol-1-2×431 kJ.mol-1=-183 KJ.mol-1
(2)c(H+)=0.1mol/L×0.1%=1×10-4,所以pH=4。酸的电离平衡常数K=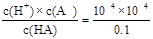 =10-7。0.1mol/L的HA溶液中由水电离出的c(H+)为10-10,所以由HA电离出来的H+的浓度约为水电离出来的H+的浓度的106倍。
=10-7。0.1mol/L的HA溶液中由水电离出的c(H+)为10-10,所以由HA电离出来的H+的浓度约为水电离出来的H+的浓度的106倍。
点评:本题综合性较强,但是难度低,比较基础。
