问题
选择题
氢氟酸是一种弱酸,可用来刻蚀玻璃。已知25 ℃时:
①HF(aq)+OH-(aq)===F-(aq)+H2O(l) 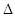 H=-67.7 kJ·mol-1
H=-67.7 kJ·mol-1
②H+(aq)+OH-(aq)===H2O(l) 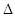 H=-57.3 kJ·mol-1
H=-57.3 kJ·mol-1
在20 mL 0.1 mol·L-1氢氟酸中加入V mL 0.1 mol·L-1 NaOH溶液,下列有关说法正确的是( )
A.氢氟酸的电离方程式及热效应可表示为:HF(aq) F-(aq)+H+(aq)
F-(aq)+H+(aq) 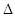 H=+10.4 kJ·mol-1
H=+10.4 kJ·mol-1
B.当V=20时,溶液中:c(OH-)=c(HF)+c(H+)
C.当V=20时,溶液中:c(F-)<c(Na+)=0.1 mol·L-1
D.当V>0时,溶液中一定存在:c(Na+)>c(F-)>c(OH-)>c(H+)
答案
答案:B
题目分析:1式—2式即可得到氟化氢电离的方程式,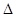 H=-10.4 kJ·mol-1故A错
H=-10.4 kJ·mol-1故A错
B.当V=20时,由于氢氟酸是弱酸,所以混合后溶液呈碱性,根据质子守恒可得c(OH-)=c(HF)+c(H+),故对。
C.当V=20时,由于混合液的体积加倍,所以物质的量的浓度降低一半,c(F-)<c(Na+)=0.05mol•L-1故错
D.当V>0时,若V=1时,由于钠离子的物质的量远远小于氟离子,所以溶液中一定不会存在:c(Na+)>c(F-)>c(OH-)>c(H+),故错
点评:本题主要考察氟化氢弱酸的电离和氟离子的水解,混合液中各离子浓度大小的比较,采用假设法可以简单快速的找到正确答案。
