问题
选择题
下列各组热化学方程式中,化学反应的△H1大于△H2的是
①C(s)+O2(g)===CO2(g) △H1; C(s)+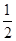 O2(g)===CO(g) △H2
O2(g)===CO(g) △H2
②2H2(g)+O2(g)==2H2O(g)△H1 ; 2H2(g)+O2(g)==2H2O(l)△H2
③H2(g)+Cl2(g)==2HCl(g)△H1 ; 1/2H2(g)+1/2Cl2(g)==HCl(g)△H2
④CaCO3(s)===CaO(s)+CO2(g) △H1 ; CaO(s)+H2O(l)===Ca(OH)2(s);△H2
A.①③
B.①④
C.②④
D.②③
答案
答案:C
题目分析:碳完全燃烧放出的热量多,但放热越多,△H越小;气态水的能量高于液态水的能量,所以氢气燃烧生成液态水放出的热量多,则选项②△H1大于△H2;参加反应的氢气越多,放出的热量越多,则选项③不符号;选项④中前者水吸热反应,后者水放热反应,△H1大于△H2,答案选C。
点评:该题是高考中的常见题型,属于中等难度的试题。试题贴近高考,基础性强,注重答题的灵活性,有利于培养学生的逻辑推理能力和发散思维能力。该题的关键是明确影响反应热大小的因素,其次还要注意反应热是有正负号的,比较时应该带着正负号比较。
