研究NO2.SO2.CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,也可用NH3处理,也可用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160 kJ·mol-1
若用标准状况下2.24L CH4还原NO2至N2整个过程中转移的电子总数为______(阿伏加德罗常数的值用NA表示),放出的热量为______kJ。
(2)已知:2SO2(g)+O2(g) 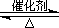 2SO3(g) ∆H=-196.6 kJ·mol-1
2SO3(g) ∆H=-196.6 kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ∆H=-113.0 kJ·mol-1
2NO2(g) ∆H=-113.0 kJ·mol-1
(ⅰ)则反应NO2(g)+SO2 (g) SO3(g)+NO(g)的∆H= kJ·mol-1。
SO3(g)+NO(g)的∆H= kJ·mol-1。
(ⅱ)一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
A.每消耗1 mol SO3的同时生成1 mol NO2 B.体系压强保持不变
C.混合气体颜色保持不变 D. SO3和NO的体积比保持不变
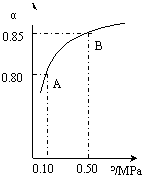
(ⅲ)某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图(左)所示。
平衡状态由A变到B时.平衡常数K(A)_______K(B)(填“>”.“<”或“=”)
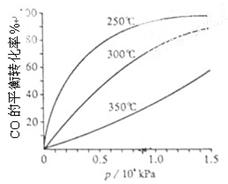
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如上图(右)所示。该反应∆H 0(填“>”或“ <”)。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如上图(右)所示。该反应∆H 0(填“>”或“ <”)。
(1)0.8NA 86.7 (2) (i)-41.8(ⅱ)C (ⅲ)= (3)<
题目分析:
(1)二式相加,除以2得到新式子:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ,每消耗0.1molCH4,转移0.8NA电子; 物质和能量是紧密相连的,以物质为基础,物质怎么变,能量就怎么变,两式直接相加,除以2,CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-173.4 kJ·mol-1,放出热量86.7kJ;
(2)(ⅰ)根据盖斯定律,将第二个方程式颠倒过来,与第一个方程式相加得:2NO2+2SO2═2SO3+2NO, △H="-83.6" kJ•mol-1,故NO2+SO2⇌SO3+NO,△H="-41.8" kJ•mol-1;(ⅱ)平衡标志,有直接标志,正逆速率相等、各组分浓度保持不变;间接标志遵循变化着的量不再改变,反应即平衡。二氧化氮为红棕色气体,颜色不再改变,反应即平衡。(ⅲ)化学平衡常数是个温度常数,温度不变,化学平衡常数不变。
(3))由图可知,温度升高,CO的转化率降低,平衡向逆反应方向移动,故逆反应是吸
热反应,正反应是放热反应,△H<0;
