(1)已知2H2(g)+O2(g)=2H2O(l)ΔH=-571.6 kJ/mol,
CO(g)+1/2O2(g)=CO2(g)ΔH=-283.0 kJ/mol。某H2和CO的混合气体完全燃烧时放出113.74 kJ热量,同时生成3.6 g液态水,则原混合气体中H2和CO的物质的量之比为___________。
(2)以甲醇、空气,氢氧化钾溶液为原料,石墨为电极,可构成燃料电池;已知该燃料电池的总反应式是:2CH3OH +3O2+4OH-=2CO32-+6H2O,该燃料电池发生反应时,正极区溶液的PH__________ (填“增大”, “减小” 或“不变”)该电池的负极反应式为_________________。
(3) 用上述燃料电池进行粗铜的精炼,粗铜应连接电源的________极,该粗铜精炼电解池的阴极反应式为_________________。
(1)1:1......2分
(2)增大….1分 CH3OH -6e-+8OH-(1)=CO32-+6H2O ....2分
(3)正…..1分。 Cu2+ + 2e- =Cu….2分
题目分析:解:水的物质的量为=0.2mol,由2H2+O2═2H2O可知,n(H2)=n(H2O)=0.2mol,由2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1可知,0.2molH2燃烧放出的热量为57.16KJ,则CO燃烧放出的热量为113.74KJ-57.16KJ=56.58KJ,设混合气体中CO的物质的量为x,则
CO(g)+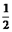 O2(g)=CO2(g)△H=-283kJ•mol-1
O2(g)=CO2(g)△H=-283kJ•mol-1
1 283KJ
X 56.58KJ
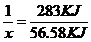
解得x=0.2mol,即n(CO)=0.20mol,则原混合气体中H2和CO的物质的量之比为1:1.(2)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池,正极反应为:3O2+12H2O+12e-=12OH-,总反应式为:2CH3OH+3O2+4OH-=2CO32-+6H2O,两式相减,负极反应为:2CH3OH-12e-+16OH-=2CO32-+12H2O,(3)和电源的正极相连的电极是阳极,电解方法精炼粗铜,电解池的阳极材料是粗铜,电极反应为:Cu-2e-=Cu2+
