碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
①已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH1= +489.0 kJ/mol
C(石墨)+CO2(g)=2CO(g) ΔH2=+172.5 kJ/mol
则CO还原Fe2O3的热化学方程式为 ;
②氯化钯(PdCl2)溶液常被应用于检测空气中微量CO。PdCl2被还原成单质,反应的化学方程式为 ;
(2)将两个石墨电极插入KOH溶液中,向两极分别通入C3H8和O2构成丙烷燃料电池。
①负极电极反应式是: ;
②某同学利用丙烷燃料电池设计了一种电解法制取Fe(OH)2的实验装置(如下图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是 (填序号)
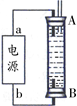
A.电源中的a一定为正极,b一定为负极
B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极
D.阴极发生的反应是:2H++2e-=H2↑
(3)将不同量的CO(g)和H2O(g)分别通入体积为2L的恒容密闭容器中,进行反应:CO(g)+H2O(g)  CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
| H2O | CO | CO2 | |||
| 1 | 650 | 2 | 4 | 1.6 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 3 |
| 3 | 900 | 1 | 2 | 0.4 | 1 |
①该反应的正反应为 (填“吸”或“放”)热反应;
②实验2中,平衡常数K= ;
③实验3跟实验2相比,改变的条件可能是 (答一种情况即可);
(4)将2.4g碳在足量氧气中燃烧,所得气体通入100mL 3.0mol/L的氢氧化钠溶液中,完全吸收后,溶液中所含离子的物质的量浓度由大到小的顺序 。
(1)①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH=﹣28.5kJ/mol
②PdCl2+CO+H2O=Pd+CO2+2HCl
(2)①C3H8-20e-+26OH-=3CO32-+17H2O ②BD
(3)① 放热 ② K=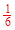 ③使用了催化剂;加大了压强
③使用了催化剂;加大了压强
(4)c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
题目分析:(1)①将第一个方程式减去3倍的第二个方程式可得目标方程式,反应热作相应的变化的即可。
②Pd被还原,则CO被氧化为CO2,根据原子守恒还应有H2O参与反应,另一种产物为HCl。
(2)①电池原理是丙烷燃烧,生成的CO2会与KOH反应生成碳酸盐。燃料电池通入燃料丙烷的一极是负极,因此负极的电极反应式为C3H8-20e-+26OH-=3CO32-+17H2O。
②用电解法制备Fe(OH)2,阳极材料用Fe,电极反应式为Fe-2e-=Fe2+,阴极溶液中的H+放电,电极反应式为2H++2e-=H2↑,电解质可用NaCl溶液。反应产生H2,使生成物处于还原氛围中,因此A、B两极都可作阳极。
(3)①实验2与实验1相比,各物质的物质的量减少一半,平衡CO2应为0.8mol,但温度升高,此时CO2的为0.4mol,说明升高温度平衡逆向移动,逆反应吸热,则正反应为放热反应。
②根据题意有:CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)
初始量/mol 1 2 0 0
变化量/mol 0.4 0.4 0.4 0.4
平衡量/mol 0.6 1.6 0.4 0.4
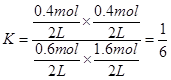
③实验3与实验2相比,平衡状态未变,但反应速率加快,因此改变的条件可能是加入催化剂或增大压强。
(4)根据题中所给的各物质的物质的量,可知反应后所得的是等物质的量的Na2CO3、NaHCO3的混合溶液,CO32-、HCO3-水解使溶液显碱性,且CO32-的水解程度大于HCO3-,因此溶液中各离子的物质的量浓度由大到小的顺序为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)。
