CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标。
(1)250℃时,以镍合金为催化剂,向4 L容器中通入6 mol CO2、6 mol CH4,发生如下反应:CO2(g)+CH4(g) 2CO(g)+2H2(g)。平衡体系中各组分体积分数如下表:
2CO(g)+2H2(g)。平衡体系中各组分体积分数如下表:
| 物质 | CH4 | CO2 | CO | H2 |
| 体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |
①此温度下该反应的平衡常数K= 。
②已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H="-890.3" kJ·mol-1
CO(g)+H2O (g)=CO2(g)+H2 (g) △H="2.8" kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H="-566.0" kJ·mol-1
反应CO2(g)+CH4(g) 2CO(g)+2H2(g) 的△H= 。
2CO(g)+2H2(g) 的△H= 。
(2)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。
①在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。250~300℃时,温度升高而乙酸的生成速率降低的原因是 。
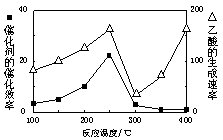
②为了提高该反应中CH4的转化率,可以采取的措施是 。
③将Cu2Al2O4溶解在稀硝酸中的离子方程式为 。
(3)以CO2为原料可以合成多种物质。
①聚碳酸酯是一种易降解的新型合成材料,它是由加聚而成。写出聚碳酸酯的结构简式: 。
②以氢氧化钾水溶液作电解质进行电解,CO2在铜电极上可转化为甲烷,该电极反应方程式为 。
(1)①64 ②+247.3 kJ·mol-1
(2)①温度超过250℃时,催化剂的催化效率降低
②增大反应压强或增大CO2的浓度
③3Cu2Al2O4+32H++2NO3-=6Cu2++ 6Al3++2NO↑+16 H2O
(3)① ②CO2+8e-+6H2O=CH4+8OH-
②CO2+8e-+6H2O=CH4+8OH-
题目分析:(1)①设消耗CH4物质的量为x,则平衡时CH4、CO2、CO、H2物质的量分别为(6-x)mol、(6-x)mol、2xmol、2xmol,由CH4体积分数得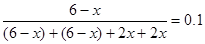 ,解得x=4。所以K=
,解得x=4。所以K= 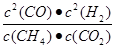 =
= 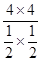 =64。②由盖斯定律得△H=(-890.3+2.8×2+566×2) kJ·mol-1=+247.3kJ·mol-1。(2)①温度升高,催化剂活性降低。②CO2(g)+CH4(g)
=64。②由盖斯定律得△H=(-890.3+2.8×2+566×2) kJ·mol-1=+247.3kJ·mol-1。(2)①温度升高,催化剂活性降低。②CO2(g)+CH4(g) CH3COOH(l),增大压强或增大二氧化碳气体浓度,可以提高甲烷转化率。③Cu2Al2O4中Cu为+1价,Cu2Al2O4与硝酸生成硝酸铜、硝酸铝、NO和水,根据得失电子相等、电荷守恒、质量守恒配平。(3)①CO2发生加聚反应时,断裂C=O双键中的
CH3COOH(l),增大压强或增大二氧化碳气体浓度,可以提高甲烷转化率。③Cu2Al2O4中Cu为+1价,Cu2Al2O4与硝酸生成硝酸铜、硝酸铝、NO和水,根据得失电子相等、电荷守恒、质量守恒配平。(3)①CO2发生加聚反应时,断裂C=O双键中的 键,聚合得
键,聚合得 。②CO2在铜电极上可转化为甲烷,C的化合价由+4降为-4,发生还原反应,由电子和电荷守恒、质量守恒写出电极反应式。
。②CO2在铜电极上可转化为甲烷,C的化合价由+4降为-4,发生还原反应,由电子和电荷守恒、质量守恒写出电极反应式。
