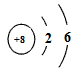(1)CH4(g )+2O2(g )=CO2(g )+2H2O(g ) ΔH=-802.3kJ/mol
该热化学反应方程式的意义是_____________________________________。
(2)已知2g乙醇完全燃烧生成液态水放出Q kJ的热量,写出表示乙醇燃烧热的热化学方
程式:____________________________________________________________.
(3)已知拆开1mol H-H键,1mol N-H键,1mol 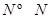 键分别需要的能量是436kJ、391KJ、946kJ,则N2与H2反应生成1mol NH3(g)的热化学方程式是___________________.
键分别需要的能量是436kJ、391KJ、946kJ,则N2与H2反应生成1mol NH3(g)的热化学方程式是___________________.
(4)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(石墨,s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol ①
2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ/mol ②
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH=-2599kJ/mol ③
根据盖斯定律,计算298K时由C(石墨,s)和H2(g)生成1mol C2H2(g)反应的焓变:
____________________________.
(1)1mol甲烷气体和2mol的氧气完全反应生成1mol二氧化碳和2mol水蒸气时放出802.3KJ的热量。(2)C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) ; ΔH=-23QKJ∕mol (3)( 1∕2) N2(g)+( 3∕2) H2(g)=NH3(g) ; ΔH=-46KJ∕mol (4)+226.7KJ∕mol。
题目分析:(1)该热化学反应方程式的意义是1mol甲烷气体和2mol的氧气完全反应生成1mol二氧化碳和2mol水蒸气时放出热量802.3KJ。(2)乙醇的相对分子质量是46.1mol乙醇的质量为46g。因为2g乙醇燃烧生成液态水放热Q kJ,所以46g乙醇燃烧生成液态水时放出的热量为23 Q kJ,所以其燃烧热的热化学方程式为:C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) ; ΔH=-23QKJ∕mol。反应热是断裂化学键吸收的能量与形学键所释放的能量差。所以N2与H2反应生成1mol NH3(g)的反应热为( 1∕2)×946+( 3∕2) ×436-3×391=-46.故该反应的热化学方程式是( 1∕2) N2(g)+( 3∕2) H2(g)=NH3(g) ; ΔH="-46KJ∕mol" (4) ①×2+(1∕2 )×②-(1∕2 )×③得ΔH=2×(-393.5)+(1∕2 )×(-571.6)+(1∕2 )×2599=+226.7KJ∕mol.。该反应的热化学方程式为:2C(石墨,s)+H2(g)=C2H2(g ) ; ΔH=+226.7KJ∕mol.