已知体积为2L的恒容密闭容器中发生反应: ,请根据化学反应的有关原理同答下列问题
,请根据化学反应的有关原理同答下列问题
(1)一定条件下,充入2 mol SO2(g)和2 mol O2(g),20 s后,测得SO2的体积百分含量为12.5%,则用SO2表示该反应在这20s内的反应速率为____,此时,该密闭容器内混合气体的压强是反应前的____倍。
(2)下面的叙述可作为判断(1)中可逆反应达到平衡状态依据的是(填序号)____。
①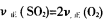
②混合气体的密度不变
③混合气体的平均相对分子质量不变
④各气体的浓度都不再发生变化
(3)下图表示该反应的速率(v)随时间(t)的变化的关系。则下列不同时间段中,SO3的百分含量最高的是( )
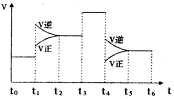

据图分析:你认为t3时改变的外界条件可能是 ;
t6时保持体积不变向体系中充人少量SO3,再次平衡后
SO2的体积百分含量比t6时 (填“大”\“小”或“等于”)。
(4)下图中P是可自由平行滑动的活塞。在相同温度时,向A容器中充入4 mol SO3(g),关闭K,向B容器中充入2 mol SO3(g),两容器分别发生反应。
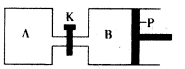
已知起始时容器A和B的体积均为aL。试回答:
①反应达到平衡时容器B的体积为1.2a L,容器B中SO3转
化率为____
②若打开K,一段时间后重新达到平衡,容器B的体积为 __L(连通管中气体体积忽略不计,且不考虑温度的影响)。
(5)已知单质硫的燃烧热为△H=-296kJ/mol,经测定由S(s)生成120gSO3(g)可放热592.5kJ,请写出SO2(g)氧化生成SO3(g)的热化学方程式____。
(1)0.04mol/(L·s)(2分) 0.8倍(2分)
(2)③④(2分)
(3)A(1分) 加入催化剂(1分) 小(1分)
(4)40℅(2分) 2.6a(2分)
(5)2SO2 (g) + O2 (g)  2SO3 (g);ΔH= -198 kJ·mol-1(2分)
2SO3 (g);ΔH= -198 kJ·mol-1(2分)
或者: SO2 (g) + 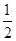 O2 (g)
O2 (g)  SO3 (g);ΔH= -99 kJ·mol-1
SO3 (g);ΔH= -99 kJ·mol-1
(1)题目分析:2SO2 + O2  2SO3,
2SO3,
始量 2mol 2mol 0 mol
变量 2xmol xmol 2xmol
平衡 (2-2x) mol (2-x) mol 2xmol
依题意有: 解之得:x=0.8mol
解之得:x=0.8mol
所以用SO2表示该反应在这20s内的反应速率为: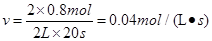
依据阿伏加德罗定律的推论:同温同体积条件下,物质的量之比等于压强之比,有:
 因此反应后的压强为反应前的0.8倍。
因此反应后的压强为反应前的0.8倍。
(2)①中这种关系在这个反应中是不管是否达到平衡状态一直存在,不正确;②中混合气体的密度也是时刻不变的,因为反应前后都是气体,质量守恒,而且体积是固定的。不正确。③该反应前后质量一定,但是正向是气体物质的量减小的方向,因此这是达到平衡的一个重要标志。正确。④各气体的浓度不再变化时,意味着各组分浓度t1是一定值,正确。
(3)t1~t2平衡逆向移动,t3~t4平衡不移动t4 ~t5平衡逆向移动,因此选A
t3~t4正逆反应速率同等程度改变,而该反应前后分子数改变,只能是加入催化剂。
体积不变时充入充人少量SO3,相当于增大压强。平衡向右移动。
(4)①题目分析:2SO3  2SO2 + O2 ,
2SO2 + O2 ,
始量 2mol 0 mol 0 mol
变量 2x mol 2x mol x mol
平衡 (2-2x) mol (0+2x) mol L (0+x) mol
依据阿伏加德罗定律的推论:同温同压条件下,物质的量之比等于体积之比,有:
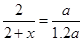 解之得:x=0.4 所以转化率为40℅
解之得:x=0.4 所以转化率为40℅
②若打开K,A和B就成了一个容器,因此再次达到平衡时的总体积应该为3×1.2aL=3.6aL,除去A中原来的1L,B的体积就应该是2.6aL。
(5) 依题意有:1 mol的S最终生成1 mol的SO3会放出592.5/1.5=395 kJ的热量。再根椐盖斯定律可知1 mol的SO2(g)氧化生成1 mol的SO3(g)能放出444-395="99" kJ的热量。因此:
2SO2 (g) + O2 (g)  2SO3 (g);ΔH= -198 kJ·mol-1
2SO3 (g);ΔH= -198 kJ·mol-1
或者:SO2 (g) + 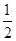 O2 (g)
O2 (g)  SO3 (g);ΔH= -99 kJ·mol-1
SO3 (g);ΔH= -99 kJ·mol-1
