人们已经研制出以丙烷为燃料的新型燃料电池,电解质为熔融碳酸盐,电池总反应方程式为:C3H8+5O2=3CO2+4H2O。
(1)已知:2C3H8(g)+7O2(g)=6CO(g)+8H2O(l)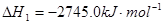
C(s)+O2(g)=CO2(g) 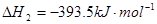
2C(s)+O2(g)=2CO(g) 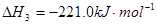
则反应C3H8(g)+5O2(g)=3CO2(g)+4H2O(1)的△H___________________。.
(2)该电池的正极通入O2和CO2,负极通入丙烷,则正极的电极反应式为_________________,电池工作时CO32—移向_____________极。
(3)用该电池电解1L 1 mol·L—1的AgNO3溶液,此电解池反应的化学方程式为______________________;当该电池消耗0.005molC3H8时,所得溶液的pH为__________(溶液体积变化忽略不计)
(1)—2221.5kJ·mol—1(2分,无单位或单位写错不给分)
(2)O2+2CO2+4e— =2CO32—(2分)负(1分)
(3)4AgNO3+2H2O 4Ag+O2↑ +4HNO3(2分,不写反应条件或不配平不给分) 1(2分)
4Ag+O2↑ +4HNO3(2分,不写反应条件或不配平不给分) 1(2分)
题目分析:(1)根据方程式先后顺序设分别为①、②、③,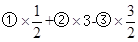 ,得到方程式C3H8(g)+5O2(g)=3CO2(g)+4H2O(1);反应热也按照上式计算△H=
,得到方程式C3H8(g)+5O2(g)=3CO2(g)+4H2O(1);反应热也按照上式计算△H=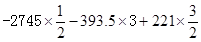 =—2221.5kJ·mol—1。
=—2221.5kJ·mol—1。
(2)氧气在正极反应,O2+2CO2+4e—=2CO32—,原电池中阴离子向负极移动;
(3)电解硝酸银,是放氧生酸型,4AgNO3+2H2O 4Ag+O2↑ +4HNO3;当该电池消耗0.005molC3H8时,转移电子是0.1mol,生成0.1molH+,氢离子浓度为0.1mol/L,pH为1。
4Ag+O2↑ +4HNO3;当该电池消耗0.005molC3H8时,转移电子是0.1mol,生成0.1molH+,氢离子浓度为0.1mol/L,pH为1。
