问题
选择题
已知:①CO(g)+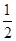 O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
②H2(g)+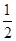 O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1
则CO(g)+H2O(g)=H2(g)+CO2(g)的ΔH为
A.+41.2 kJ•mol-1
B.-41.2 kJ•mol-1
C.+82.4kJ•mol-1
D.-524.8 kJ•mol-1
答案
答案:B
题目分析:已知:①CO(g)+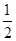 O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1,②H2(g)+
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1,②H2(g)+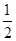 O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1,则根据盖斯定律可知①-②即得到反应CO(g)+H2O(g)=H2(g)+CO2(g),所以该反应的反应热ΔH=-283.0 kJ·mol-1+241.8 kJ·mol-1=-41.2 kJ•mol-1,所以答案选B。
O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1,则根据盖斯定律可知①-②即得到反应CO(g)+H2O(g)=H2(g)+CO2(g),所以该反应的反应热ΔH=-283.0 kJ·mol-1+241.8 kJ·mol-1=-41.2 kJ•mol-1,所以答案选B。
