氨有着广泛的用途,可用于化肥、硝酸、合成纤维等工业生产。
(1)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应可生成氨气:
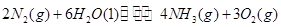
该反应在固定体积的密闭容器中进行,有关说法正确的是_____________(填序号字母)。
A.反应处于平衡状态时,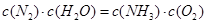
B.反应达到平衡后,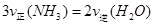
C.体系的总压强不变,说明反应已达平衡
D.混合气体的密度保持不变,说明反应已达平衡(2)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视。它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。氨在燃烧试验机中相关的反应有:
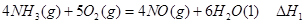 ①
①
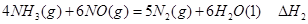 ②
②
 ③
③
请写出上述三个反应中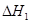 、
、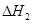 、
、 三者之间关系的表达式,
三者之间关系的表达式, =_________。
=_________。
(3)工业制硝酸的主要反应是: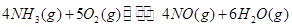
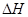 =
=
①升高温度,反应的K值减小,则Q______(填“>”、“<”或“=”)0。
②若反应起始的物质的量相同,下列关系图错误的是________(填序号)。


③在容积固定的密闭容器中发生上述反应,容器内部分物质的浓度如下表:
| 时间/浓度 | 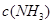
| 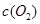
| 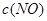
| 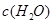
|
| 起始 | 4.0 | 5.5 | 0 | 0 |
| 第2min | 3.2 | a | 0.8 | 1.2 |
| 第4min | 2.0 | 3.0 | 2.0 | 3.0 |
| 第6min | 2.0 | 3.0 | 2.0 | 3.0 |
反应在第2 min到第4 min时,O2的平均反应速率为________。
反应在第2 min时改变了条件,改变的条件可能是______________________________。
该条件下,反应的平衡常数K=________。
(1)CD(2分)
(2)△H3=(3△H1+2△H2)/5(2分)
(3)①<(2分) ②AC(2分)
③0.75 mol·L-1·min-1(2分) 使用催化剂或升高温度(2分) 3.0(2分)
题目分析:(1)反应处于平衡状态时,体系中各组分的浓度不变,与c(NH3)·c(O2)和c(NO)·c(H2O)是否相等无关;反应达到平衡后,则一定有3v正(NH3)=2v逆(H2O);反应前后气体的物质的量不相等,总压不变,可说明反应已达平衡;反应达到平衡后,混合气体的质量保持不变,说明反应已达平衡。(2)第三个反应中无NO,①×3+②×2可消去NO,然后除以5就可由①②两式得到③式。即:△H3=(3△H1+2△H2)/5。(3)①反应的K值减小,证明升温平衡逆向移动,因而正反应放热,Q<0。②温度升高,平衡逆向移动,NH3的含量增大,H2O的含量降低,A、C错误;压强增大,反应速率加快,平衡逆向移动,NO的含量降低,B正确;加入催化剂,反应速率加快,平衡不移动,D正确。③第2 min到第4 min,NH3的浓度变化了1.2 mol·L-1,因而O2的浓度变化了1.2mol·L-1 ×5÷4=1.5 mol·L-1,其平均反应速率为0.75 mol·L-1·min-1。根据物质之间的浓度关系,不可能是加入了物质或减小了体积,但反应速率确实加快了,因而可能是使用了催化剂或升高了温度。由于第4 min到第6 min,反应混合物的浓度不再变化,因而已经达到平衡,将相关数据代入K= ,得K=3。
,得K=3。