氯化铁是一种重要的化工原料,无水氯化铁遇潮湿空气极易吸水生成FeCl3·nH2O。
(1)实验室用如下装置(部分加热、夹持等装置已略去)制备无水氯化铁固体。
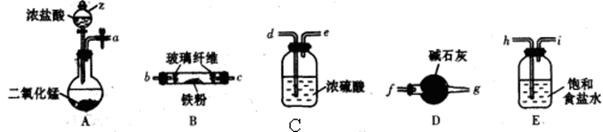
①装置A中仪器z的名称是___________。
②简述检验装置A气密性的操作:______________________。
③按气流方向连接各仪器接口,顺序为a→_________ →__________ →_________ →__________→b→c→_________→__________,装置D的作用是______________________。
(2)工业上制备无水氯化铁的一种工艺流程如下:
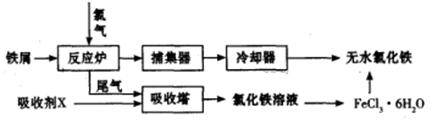
①吸收塔中发生反应的离子方程式为_________________________________________。
②简述由FeCl3·6H2O晶体得到无水氯化铁的操作:________________________________。
③用碘量法测定所得无水氯化铁的质量分数:称取m克无水氯化铁样品,溶于稀盐酸,再转移到100 mL容量瓶中,用蒸馏水定容;取出10 mL,加入稍过量的KI溶液,充分反应后,滴入指示剂_________(填试剂名称),用c mol/L的Na2S2O3溶液进行滴定,终点时消耗V mLNa2S2O3溶液(已知:I2+2S2O32-=2I-+S4O62-)。则样品中氯化铁的质量分数为____________。
(3)若已知:
Fe(OH)3(aq) Fe3+(aq)+3OH-(aq) △H=a kJ/mol
Fe3+(aq)+3OH-(aq) △H=a kJ/mol
H2O(l) H+(aq)+OH-(aq) △H=b kJ/mol
H+(aq)+OH-(aq) △H=b kJ/mol
请写出Fe3+发生水解反应的热化学方程式________________________________________。
(16分)(1)①分液漏斗(1分,写错字不得分)
②关闭a处弹簧夹和分液漏斗的活塞,向分液漏斗中加入较多的水,然后打开分液漏斗的活塞,使水缓缓流下,若分液漏斗中的水不能完全漏下,说明装置气密性好(或在a管处接一导管,并将导管末端插入水中,同时关闭分液漏斗的活塞,用酒精灯给圆底烧瓶微热,若导管末端有气泡冒出,停止加热恢复室温时,导管末端形成一小段水柱,说明装置气密性好。(2分,合理答案即可)③a→h→i→d→e→b→c→f→g (2分,顺序写错不得分) 吸收未反应的Cl2 (1分),同时防止空气中的水蒸气进入装置B (1分) (共2分,合理答案即可)
(2)①2Fe2++Cl2=2Fe3++2Cl- (2分,化学式写错、不配平均不得分,写化学方程式不得分)
②将FeCl3·6H2O晶体置于HCl气流中加热(2分,合理答案即可)
③淀粉溶液或淀粉 (1分) 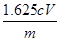 %或
%或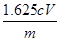 或
或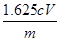 ×100% (2分,合理答案即可)
×100% (2分,合理答案即可)
(3)Fe3+(aq)+3H2O(l) Fe(OH)3(aq) + 3H+(aq) △H=(3b-a)kJ·mol-1 (2分,化学式写错、表达式写错、不配平、漏写物质状态、漏写单位均不得分)
Fe(OH)3(aq) + 3H+(aq) △H=(3b-a)kJ·mol-1 (2分,化学式写错、表达式写错、不配平、漏写物质状态、漏写单位均不得分)
题目分析:(1)①根据装置的结构特点可判断,装置A中仪器z的名称是分液漏斗;
②装置气密性检验一般是借助于气压差,因此根据该装置的特点可知,检验装置A气密性的操作应该是关闭a处弹簧夹和分液漏斗的活塞,向分液漏斗中加入较多的水,然后打开分液漏斗的活塞,使水缓缓流下,若分液漏斗中的水不能完全漏下,说明装置气密性好(或在a管处接一导管,并将导管末端插入水中,同时关闭分液漏斗的活塞,用酒精灯给圆底烧瓶微热,若导管末端有气泡冒出,停止加热恢复室温时,导管末端形成一小段水柱,说明装置气密性好。
③由于无水氯化铁遇潮湿空气极易吸水生成FeCl3·nH2O,而制得的氯气中含有水蒸气和氯化氢,所以在和铁反应之前需要净化氯气。氯化氢用饱和食盐水除去,浓硫酸用来干燥氯气,且首先除去氯化氢,最后干燥。同时为了防止氯气污染空气,且也为了防止空气中的水蒸气进入反应器,还需要有尾气处理装置,选择的装置是盛有碱石灰的干燥管,所以正确的连接顺序为a→h→i→d→e→b→c→f→g;根据以上分析可知,装置D的作用是吸收未反应的Cl2,同时防止空气中的水蒸气进入装置B。
(2)①从吸收塔中出来的是氯化铁溶液,所以吸收剂X应该是氯化亚铁,所以该反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-;
②由于氯化铁水解生成氢氧化铁和氯化氢,水解吸热,且生成的 氯化氢极易挥发,进一步促进水解,所以由FeCl3·6H2O晶体得到无水氯化铁的操作应该是将FeCl3·6H2O晶体置于HCl气流中加热;
③氯化铁能把碘化钾氧化生成单质碘,而碘遇淀粉显蓝色,所以加入的指示剂应该是淀粉溶液;根据方程式2Fe3++2I-=2Fe2++I2、I2+2S2O32-=2I-+S4O62-可知2Fe3+~I2~2S2O32-,则10ml溶液中铁离子的物质的量是0.001cVmol,所以原样品中氯化铁的物质的量是0.001cVmol×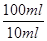 =0.01cVmol,因此氯化铁的质量是0.01cVmol×162.5g/mol=1.625cVg,则样品中氯化铁的质量分数为
=0.01cVmol,因此氯化铁的质量是0.01cVmol×162.5g/mol=1.625cVg,则样品中氯化铁的质量分数为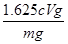 ×100%=
×100%=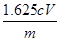 %。
%。
(3)已知①Fe(OH)3(aq) Fe3+(aq)+3OH-(aq) △H=a kJ/mol,②H2O(l)
Fe3+(aq)+3OH-(aq) △H=a kJ/mol,②H2O(l) H+(aq)+OH-(aq) △H=b kJ/mol,则根据盖斯定律可知②×3-①即得到方程式)Fe3+(aq)+3H2O(l)
H+(aq)+OH-(aq) △H=b kJ/mol,则根据盖斯定律可知②×3-①即得到方程式)Fe3+(aq)+3H2O(l) Fe(OH)3(aq) + 3H+(aq),所以该反应的反应热△H=(3b-a)kJ·mol-1。
Fe(OH)3(aq) + 3H+(aq),所以该反应的反应热△H=(3b-a)kJ·mol-1。
