(1)合成氨反应的热化学方程式:N2(g)+3H2(g) 2NH3(g)ΔH=-92.2kJ·mol-1
2NH3(g)ΔH=-92.2kJ·mol-1
已知合成氨反应是一个反应物不能完全转化为生成物的反应,在某一定条件下,N2的转化率仅为10%,要想通过该反应得到92.2 kJ的热量,至少在反应混合物中要投放N2的物质的量为________ mol。
(2)肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼-空气燃料电池放电时:
正极的电极反应式:__________________________,
负极的电极反应式:__________________________。
(3)如图是一个电解过程示意图。

①锌片上发生的电极反应式是:_______________________
②假设使用肼-空气燃料电池作为该过程中的电源,铜片质量变化为128 g,则肼-空气燃料电池理论上消耗标准状况下的空气________L(假设空气中氧气体积分数为20%)。
(1)10
(2)O2+4e-+2H2O=4OH-
N2H4+4OH--4e-=4H2O+N2↑
(3)①Cu2++2e-=Cu ②112
(1)据热化学方程式可知,1 mol N2完全反应才能得到92.2 kJ的热量,而N2
转化率为10%,则实际需要投入10 mol N2才能转化1 mol N2。
(2)肼-空气燃料电池中,O2在正极放电,生成OH-。
(3)电解池中,Cu做阳极,自身放电生成Cu2+,由电子守恒得Cu~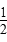 O2~2e-,n(Cu)
O2~2e-,n(Cu)
=2 mol,消耗n(O2)=1 mol,则V空气=112 L(标准状况)。
