以CO2为碳源制取低碳有机物成为国际研究焦点,下面为CO2加氢制取低碳醇的热力学数据:
反应Ⅰ: CO2(g)+3H2(g) CH3OH(g)+H2O(g) ∆H = —49.0 kJ·mol-1
CH3OH(g)+H2O(g) ∆H = —49.0 kJ·mol-1
反应Ⅱ:2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) ∆H = —173.6 kJ·mol-1
CH3CH2OH(g)+3H2O(g) ∆H = —173.6 kJ·mol-1
(1)写出由CH3OH(g)合成CH3CH2OH(g)的热化学反应方程式:
(2)对反应Ⅰ,在一定温度下反应达到平衡的标志是 (选填编号)
a.反应物不再转化为生成物 b.平衡常数K不再增大
c.CO2的转化率不再增大 d.混合气体的平均相对分子质量不再改变
(3)在密闭容器中,反应Ⅰ在一定条件达到平衡后,其它条件恒定,能提高CO2转化率的措施是 (选填编号)
A.降低温度
B.补充CO2
C.加入催化剂
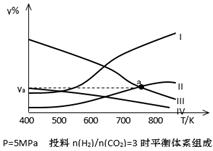
D.移去甲醇(4)研究员以生产乙醇为研究对象,在密闭容器中,按H2与CO2的物质的量之比为3:1进行投料,在5MPa下测得不同温度下平衡体系中各种物质的体积分数(y%)如下图所示。表示CH3CH2OH组分的曲线是 ;图中曲线Ⅱ和Ⅲ的交点a对应的体积分数ya= %(计算结果保留三位有效数字)
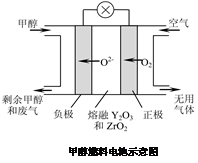
(5)一种以甲醇作燃料的电池示意图如图。写出该电池放电时负极的电极反应式: 。
(1)2CH3OH(g)  CH3CH2OH(g) +H2O(g) ∆H = —75.6 kJ·mol-1(3分)
CH3CH2OH(g) +H2O(g) ∆H = —75.6 kJ·mol-1(3分)
(2)cd(2分)
(3)AD(2分)
(4) Ⅳ(2分) 18.8(3分)
(5)CH3OH-6e-+3O2-=CO2↑+2H2O(3分)
题目分析:(1)根据盖斯定律,将反应Ⅰ×2,然后用反应Ⅱ减去反应Ⅰ×2即得所求方程式。所以由CH3OH(g)合成CH3CH2OH(g)的热化学反应方程式2CH3OH(g)  CH3CH2OH(g) +H2O(g) ∆H = —75.6 kJ·mol-1
CH3CH2OH(g) +H2O(g) ∆H = —75.6 kJ·mol-1
(2)a、化学平衡是动态平衡,反应一直进行,错误;b、温度不变,化学平衡常数不变,所以一定温度下的平衡常数一直不变,错误;c、反应开始时二氧化碳的转化率一直升高,达平衡时转化率不再升高,正确;d、该反应是反应前后气体的物质的量改变的可逆反应,气体总质量不变,所以混合气体的平均相对分子质量一直在变化,达平衡时不再变化,正确,答案选cd。
(3)提高CO2转化率也就是使平衡正向移动,A、降温,平衡向放热反应方向移动,正反应为放热反应,所以平衡正向移动,正确;B、补充二氧化碳只能提高氢气的转化率,本身的转化率降低,错误;C、加入催化剂对平衡无影响,错误;D、移走甲醇,使生成物浓度减小,平衡正向移动,正确,答案选AD。
(4)升高温度,平衡逆向移动,二氧化碳与氢气的含量增大,乙醇与水的含量减小,反应开始时按H2与CO2的物质的量之比为3:1进行投料,所以生成的乙醇与水的物质的量比仍为1:3,即水的含量是乙醇含量的3倍,所以表示CH3CH2OH组分的曲线是Ⅳ;曲线曲线Ⅱ和Ⅲ分别代表二氧化碳、水,当二者的体积分数相同时,体积也相同,设它们的体积都是V,根据投料比,氢气的体积是二氧化碳的3倍为3V,乙醇的体积是水的1/3,即1/3V,所以总体积是V+V+3V+1/3V=16V/3,则a点对应的体积分数ya=V/16V/3×100%=18.75%;保留3位有效数字是18.8%。
(5)甲醇燃料电池中在负极发生氧化反应的是甲醇,结合正极产生的氧负离子生成二氧化碳和水,电极反应式CH3OH-6e-+3O2-=CO2↑+2H2O
